
(10广州25)硫酸钠是制造纸浆、燃料稀释剂、医药用品等的重要原料。某硫酸钠粗品中含有少量的氯化钙、氯化镁,实验室进行提纯的流程如下:
回答下列问题:
(1)用氢氧化钠和碳酸钠除杂时,反应的化学方程式分别为 、
(2)氢氧化钠和碳酸钠如果要添加过量了,可加入适量 溶液除去。
(3)“后续处理”的主要操作时蒸发,为了获得纯净的硫酸钠,应蒸发至 (填序号)。
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(4)已知硫酸钠的溶解度随温度变化的曲线如右图所示。40℃时,100g蒸馏水中溶解 g硫酸钠达到饱和。将该饱和溶液升高温度至90℃,观察到的现象是 。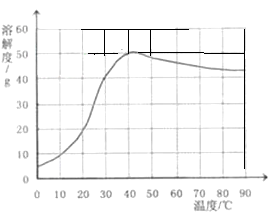
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
(10广州25)硫酸钠是制造纸浆、燃料稀释剂、医药用品等的重要原料。某硫酸钠粗品中含有少量的氯化钙、氯化镁,实验室进行提纯的流程如下:
回答下列问题:
(1)用氢氧化钠和碳酸钠除杂时,反应的化学方程式分别为 、
(2)氢氧化钠和碳酸钠如果要添加过量了,可加入适量 溶液除去。
(3)“后续处理”的主要操作时蒸发,为了获得纯净的硫酸钠,应蒸发至 (填序号)。
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
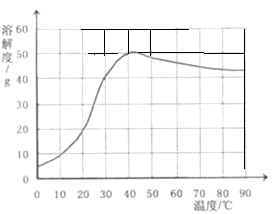
(4)已知硫酸钠的溶解度随温度变化的曲线如右图所示。40℃时,100g蒸馏水中溶解 g硫酸钠达到饱和。将该饱和溶液升高温度至90℃,观察到的现象是 。
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源:2010年全国中考真题分类汇编专题三物质的分离与提纯 题型:填空题
(10广州25)硫酸钠是制造纸浆、燃料稀释剂、医药用品等的重要原料。某硫酸钠粗品中含有少量的氯化钙、氯化镁,实验室进行提纯的流程如下:
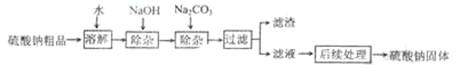
回答下列问题:
(1)用氢氧化钠和碳酸钠除杂时,反应的化学方程式分别为 、
(2)氢氧化钠和碳酸钠如果要添加过量了,可加入适量 溶液除去。
(3)“后续处理”的主要操作时蒸发,为了获得纯净的硫酸钠,应蒸发至 (填序号)。
A.完全蒸干时停止加热
B.快干时停止加热,利用余热蒸干
C.有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(4)已知硫酸钠的溶解度随温度变化的曲线如右图所示。40℃时,100g蒸馏水中溶解 g硫酸钠达到饱和。将该饱和溶液升高温度至90℃,观察到的现象是 。

查看答案和解析>>
科目:初中化学 来源:2010年全国中考真题专题汇编专题六化学方程式计算(一) 题型:计算题
(10广东省25)氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气和氢
氧化钠等物质,发生的化学反应如下:2NaCl + 2H2O Cl2 ↑+ H2
↑+ 2NaOH。现取100g
Cl2 ↑+ H2
↑+ 2NaOH。现取100g
的溶质质量分数为25%的氯化钠溶液进行电解,一段时间后停止通电,生成氯气的质量7.1g。
请计算:
(1)生成氢气的质量是多少?剩余氯化钠的质量是多少?
(2)反应后溶液中NaOH的质量分数是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com