
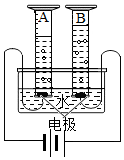
 如图是一个电解水的装置,其中A中产生的是氢气气体,电解水实验的文字表达式是水$\stackrel{通电}{→}$氢气+氧气.
如图是一个电解水的装置,其中A中产生的是氢气气体,电解水实验的文字表达式是水$\stackrel{通电}{→}$氢气+氧气. 科目:初中化学 来源: 题型:解答题
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | |
| 溶解度(g) | A | 35 | 35.5 | 36 | 36.5 | 37 |
| B | 6 | 10 | 18 | 36.5 | 50 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲酸是由碳、氢、氧三种元素组成的有机物 | |
| B. | 甲酸中有一个碳原子、两个氢原子和两个氧原子 | |
| C. | 甲酸中碳、氢、氧三种原子的个数比为1:2:2 | |
| D. | 甲酸中碳、氢、氧三种元素的质量比为6:1:16 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 检验食盐中是否含有氯元素 | B. | 检验自来水是否用氯气消毒 | ||
| C. | 检验鸡蛋壳是否可溶于酸 | D. | 确定味精的元素组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
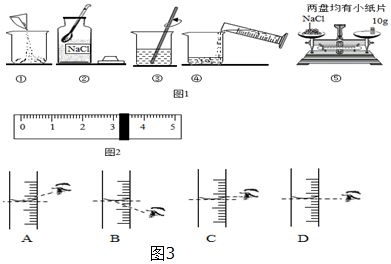
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
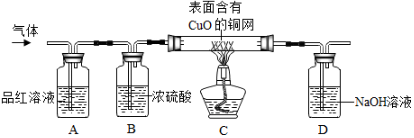

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
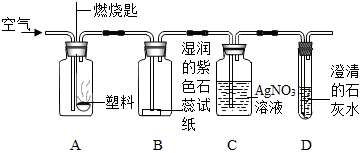
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com