
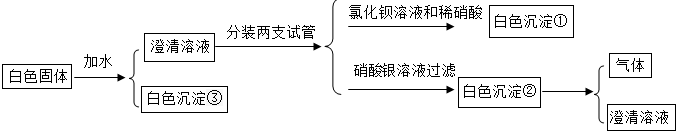
分析 碳酸钙不溶于水;
硫酸钠能和氯化钡反应生成硫酸钡沉淀和氯化钠,硫酸钡不溶于水和稀硝酸;
硝酸银能和氯化钙反应生成氯化银沉淀和硝酸钙,氯化银不溶于水和稀硝酸;
碳酸钾能和硝酸银反应生成碳酸银沉淀和硝酸钾,碳酸银能和稀硝酸反应生成硝酸银、水和二氧化碳.
解答 解:向澄清溶液中加入氯化钡溶液和稀硝酸时,能够生成白色沉淀,该白色沉淀不溶于稀硝酸,是硫酸钠和氯化钡反应生成的硫酸钡沉淀,因此白色粉末中一定含有硫酸钠;
向澄清溶液中加入硝酸银溶液时,能够生成白色沉淀,该白色沉淀能和稀硝酸反应,说明不是氯化银,即白色粉末中不含有氯化钙,该沉淀是碳酸钾和硝酸银反应生成的碳酸银,因此白色粉末中一定含有碳酸钾;
因为白色粉末中不含有氯化钙,则白色粉末加水后得到的白色沉淀不是反应生成的碳酸钙,而是原白色粉末中含有碳酸钙;
实验过程中,是否含有硝酸钾,不影响实验过程,因此白色粉末中可能含有硝酸钾,也可能不含有硝酸钾;
(1)原固体混合物中一定有碳酸钙、硫酸钠和碳酸钾,可能有硝酸钾,一定没有氯化钙;
(2)白色沉淀①②分别是硫酸钡、碳酸银;
(3)白色沉淀②是碳酸银,与稀硝酸发生反应的化学方程式为:Ag2CO3+2HNO3=2AgNO3+H2O+CO2↑;
(4)白色沉淀③一定是碳酸钙,来源于白色粉末;
小明同学则认为来源于氯化钙与碳酸钾反应所得是不正确的,因为白色粉末中不含有氯化钙.
故填:碳酸钙、硫酸钠和碳酸钾;硝酸钾;氯化钙;硫酸钡;碳酸银;Ag2CO3+2HNO3=2AgNO3+H2O+CO2↑;白色粉末;白色粉末中不含有氯化钙.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


科目:初中化学 来源: 题型:选择题
| A. | 水在通电的条件下能分解成氢气和氧气--分子是化学变化中的最小粒子 | |
| B. | 湿衣服在阳光下晒干--分子在不断地运动 | |
| C. | 100mL的水和100mL的酒精混合后,体积小于200mL--分子之间有间隙 | |
| D. | 一滴水中大约有1.67×1021个水分子--分子的质量和体积都很小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 小刚学完酸碱盐知识后设计了以下试验,仔细观察你能看到什么现象?(任答三种现象)(提示:某些非金属氧化物能和水反应生成酸,如CO2+H2O═H2CO3)
小刚学完酸碱盐知识后设计了以下试验,仔细观察你能看到什么现象?(任答三种现象)(提示:某些非金属氧化物能和水反应生成酸,如CO2+H2O═H2CO3)查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com