



科目:初中化学 来源: 题型:
| W | X | Y | Z | |
| 稀盐酸 | × | √ | × | √ |
| Z(NO3)2溶液 | × | √ | × | |
| YNO3溶液 | √ | √ |
查看答案和解析>>
科目:初中化学 来源: 题型:

| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:
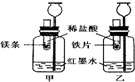 人类的生产生活离不开金属.(1)在地壳里含量居第二位的金属元素是
人类的生产生活离不开金属.(1)在地壳里含量居第二位的金属元素是查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
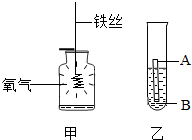 人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.
人类的生产生活离不开金属,下列三种金属被发现、使用的先后顺序依次为:铜、铁、铝.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com