
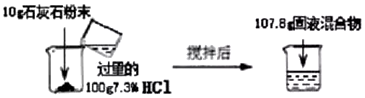
���� ��1������������������ԭ���������㣻
��2������̼�����ϡ���ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼д����Ӧ�Ļ�ѧ����ʽ��
��3�����������غ㶨�ɣ��ձ��ڼ��ٵ����������ɵĶ�����̼�������ݴ˸��ݷ�Ӧ�Ļ�ѧ����ʽ�г�̼��������ı���ʽ�����̼��Ƶ��������Ȼ��Ƶ����������ʯ��ʯ��̼�������������
��4�������������������������Һ���Ȼ��Ƶ�����������
��� �⣺��1����������������ԭ�����������������ļ��㹫ʽ��֪����Ҫ��������Ϊ36.5%��Ũ�����������
$\frac{100g��7.3%}{36.5%}$=20g��
��2���������غ㶨�ɣ����ɶ�����̼������Ϊ100g+10g-107.8g=2.2g��
��μӷ�Ӧ̼��Ƶ�����Ϊx�������Ȼ��Ƶ�����Ϊy��
CaCO3+2HCl=CaCl2+H2O+CO2��
100 111 44
x y 2.2g
$\frac{100}{44}=\frac{x}{2.2g}$ ��ã�x=5g
$\frac{111}{44}=\frac{y}{2.2g}$ ��ã�y=5.55g
ʯ��ʯ��̼�����������Ϊ��$\frac{5g}{10g}��100%$=50%��
��3����Һ���Ȼ��Ƶ����������ǣ�$\frac{5.55g}{5g+100g-2.2g-2.8g}��100%$=5.55%��
�ʴ�Ϊ����l��20g����2��CaCO3+2HCl=CaCl2+CO2��+H2O����3��$\frac{100}{44}=\frac{x}{2.2g}$��50%�� ��4��5.55%��
���� �����ѶȲ������ո��ݻ�ѧ����ʽ�ļ��㼴����ȷ����⣬���������غ㶨�ɼ����������̼����������ȷ������ǰ��ؼ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ǽ������� | B�� | ����Ĥ�������� | ||
| C�� | ������˿���ںϳɲ��� | D�� | ���������ڸ��ϲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2 | B�� | HClO | C�� | HCl | D�� | N2O5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����� | B�� | ����� | C�� | �������� | D�� | ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | �� | C�� | ���� | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe Hg | B�� | Fe Zn | C�� | Cu Hg | D�� | Cu Zn |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
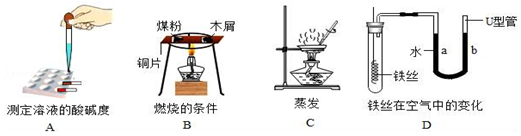
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com