
【题目】化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究。
(1)【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】为保证实验准确性,实验所用金属片均用砂纸打磨,打磨目的主要是:。
实验⑴为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡。写出锌与盐酸发生反应的化学方程式为。
从实验现象可判断:金属活动性ZnFe(填“<”、“=”或“>”)。
【得出结论1】
金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是。
(2)实验⑵为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是。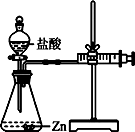
所用药品、实验数据如下表:
实验 | 选用金属 | 盐酸质量分数 | 每分钟产生氢气的体积/mL | |||||
1分钟 | 1﹣2 | 2﹣3 | 3﹣4 | 4﹣5 | 前5分 | |||
Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【得出结论2】金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是。
(3)【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快原因:再由快到慢的原因是。
(4)【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?
因素1:。
因素2:。
【答案】
(1)去除表面氧化物及杂质;Zn+2HCl=ZnCl2+H2↑;>;金属活动性越强,反应越剧烈
(2)通过注射器往右移动的体积测得生成氢气的体积;其他条件相同时,盐酸浓度越大,反应越剧烈
(3)锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快;一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢
(4)固体的表面积、反应物的状态;催化剂的影响
【解析】(1)【设计探究】由于金属在存放过程中金属可能生锈或者有污物。故实验所用金属片均用砂纸打磨,打磨目的主要是:去除表面氧化物及杂质;
由题意知:反应物、生成物,根据质量守恒定律,正确书写化学方程式;如锌与盐酸反应:反应物为锌与盐酸,生成物为氯化锌与氢气,根据质量守恒定律,故正确书写化学方程式Zn+2HCl=ZnCl2+H2↑;
放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,金属活动性Zn>Fe;
得出结论1:根据金属的活动性顺序,金属的活动性与反应的剧烈程度的关系是金属活动性越强,反应越剧烈;
(2)实验(2)注射器的作用是通过注射器往右移动的体积测得生成氢气的体积;
得出结论2:其他条件相同时,盐酸浓度越大,反应越剧烈;
(3)【反思评价】锌与盐酸反应产生气体的速度先加快后变慢,因为锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快,再由快到慢的原因是一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢;
(4)【拓展延伸】金属与盐酸反应的剧烈程度可能受固体的表面积、反应物的状态、催化剂的影响.
故答案为:(1)去除表面氧化物及杂质;Zn+2HCl=ZnCl2+H2↑;>;金属活动性越强,反应越剧烈;(2)通过注射器往右移动的体积测得生成氢气的体积;其他条件相同时,盐酸浓度越大,反应越剧烈;(3)锌与稀盐酸反应放热,随着反应的进行,温度升高,所以速度越来越快;一段时间后,盐酸被消耗,盐酸浓度变小,反应速率减慢;(4)固体的表面积、反应物的状态;催化剂的影响.
(1)【设计探究】金属在存放过程中金属可能生锈或者有污物;锌和稀盐酸反应生成氯化锌和氢气;根据锌和铁与酸反应的剧烈程度可判断它们的活动性强弱;
(2)注射器的作用是量取生成气体的体积;
得出结论:根据表中信息结合浓度对反应的影响分析解答;
(3)【反思评价】根据表中信反应的剧烈程度与酸的浓度有关;
(4)根据控制变量法结合影响反应速率的因素进行设计实验即可.


科目:初中化学 来源: 题型:
【题目】下列叙述正确的是
A.人体缺乏铁元素会引起贫血,所以我们应该适量补铁
B.将生锈的菜刀浸泡在食盐水中,可除去其表面的铁锈
C.用甲醛溶液浸泡鲜虾仁
D.用清洗过的霉变大豆榨豆浆
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列所示图象能正确反映对应的实验或化学反应事实的是( )
A. 稀H2SO4滴入BaCl2溶液中
稀H2SO4滴入BaCl2溶液中
B.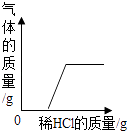 往部分变质的NaOH溶液中滴加稀盐酸
往部分变质的NaOH溶液中滴加稀盐酸
C.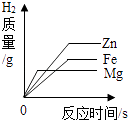 等质量的Mg、Zn、Fe与足量的等质量分数的稀盐酸反应
等质量的Mg、Zn、Fe与足量的等质量分数的稀盐酸反应
D.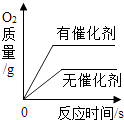 等质量,等质量分数的过氧化氢溶液制取O2
等质量,等质量分数的过氧化氢溶液制取O2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验现象描述不正确的是()
A.硫在空气中燃烧产生淡蓝色火焰
B.木炭在氧气中剧烈燃烧,生成二氧化碳
C.红磷在空气中燃烧产生大量白烟
D.电解水一段时间后,正负极产生气体的体积比约为1:2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】安徽芜湖轻轨2016年底开工建设,这也标志着,未来芜湖市民将迎来“轻轨生活”,改变出行方式,如图是芜湖轻轨图:
(1)所标部件中,属于金属材料的是(填序号),属于有机合成材料的是(填序号)。
(2)铝的活动性比铁(填“强”或“弱”),请用一个化学方程式表示:。
(3)轻轨的投入使用对环境有什么意义?。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com