
| 100 |
| x |
| 44 |
| 22g |
| 50g |
| 53g |


科目:初中化学 来源: 题型:
| A、将软水变为硬水的方法是煮沸 |
| B、农药、化肥的不合理施用,会造成水体污染 |
| C、生活污水经过净化处理后再排放 |
| D、水是一种最常用的溶剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
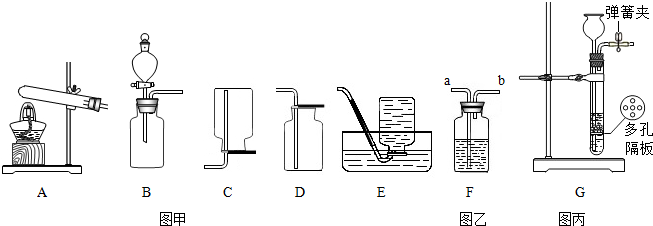
查看答案和解析>>
科目:初中化学 来源: 题型:
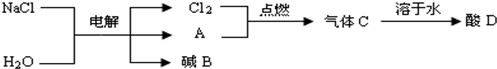
查看答案和解析>>
科目:初中化学 来源: 题型:
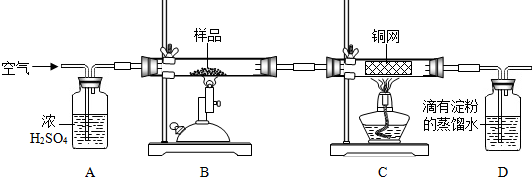
| 1 |
| 10 |
查看答案和解析>>
科目:初中化学 来源: 题型:
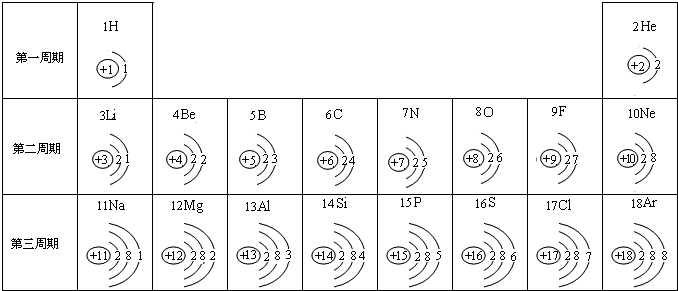
 写离子符号
写离子符号查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com