
·ÖĪö øł¾ŻĒāŃõ»ÆÄĘŗĶŃĪĖį·“Ӧɜ³ÉĀČ»ÆÄĘŗĶĖ®£¬ĒāŃõ»ÆÄĘŗĶĮņĖį·“Ӧɜ³ÉĮņĖįÄĘŗĶĖ®£¬ÕŅ³ö¹ŲĻµŹ½£¬Č»ŗó½įŗĻĢāÖŠµÄŹż¾Ż¼ĘĖć£®
½ā“š ½ā£ŗÉč“óŌ¼ŠčŅŖĻ”ĮņĖįxµĪ£¬
NaOH+HCl=NaCl+H2O 2NaOH+H2SO4=Na2SO4+2H2O
ĖłŅŌ 2HCl-----H2SO4
73 98
20”Į0.05mL”Į1.00g/mL x”Į0.05mL”Į1.00g/mL
$\frac{73}{20”Į0.05mL”Į1.00g/mL}$=$\frac{98}{x”Į0.05mL”Į1.00g/mL}$
x=27
¹Ź“š°øĪŖ£ŗ27£®
µćĘĄ ±¾ĢāÖ÷ŅŖæ¼²éĮĖÖŠŗĶµĪ¶Ø²Ł×÷ŅŌ¼°¼ĘĖć£¬ÄŃ¶Č²»“ó£¬Ąķ½āÖŠŗĶµĪ¶ØµÄŌĄķŹĒ½āĢā¹Ų¼ü£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
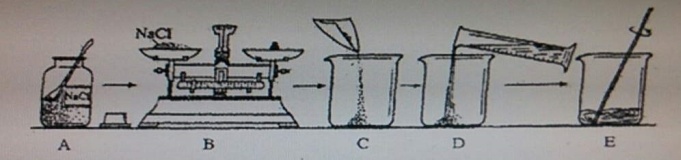
| ŹµŃé²½Öč | ŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
| ȔɣĮæÉÕ±ÄŚČÜŅŗÓŚŹŌ¹ÜÖŠ£¬µĪČė¼øµĪ·ÓĢŖČÜŅŗ£¬Õńµ“ | ČÜŅŗĪŽĆ÷ĻŌ±ä»Æ»ņČÜŅŗ²»±äŗģÉ« | ²ĀĻėŅ»²»ÕżČ· |
| ĮķȔɣĮæÉÕ±ÄŚČÜŅŗÓŚĮķŅ»Ö§ŹŌ¹ÜÖŠ£¬ÖšµĪ¼ÓČėĢ¼ĖįÄĘČÜŅŗÖĮ¹żĮæ | ĻČÓŠĘųĢå²śÉś£¬ŗó²śÉś³Įµķ | ²ĀĻė¶ž²»ÕżČ· ²ĀĻėČżÕżČ· |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗģÄ«Ė®±Ź | B£® | “æĄ¶Ä«Ė®±Ź | C£® | Ģ¼ĖŲÄ«Ė®±Ź | D£® | Ō²Ö鱏 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŠņŗÅ | ¼ÓČėĻ”ŃĪĖįµÄÖŹĮæ£Øg£© | Ź£Óą¹ĢĢåµÄÖŹĮæ£Øg£© |
| 1 | 25 | 5.5 |
| 2 | 25 | m |
| 3 | 25 | 1.2 |
| 4 | 25 | n |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
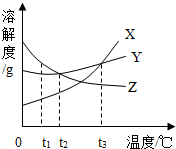 ČēĶ¼ŹĒX”¢Y”¢ZČżÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻßĶ¼£¬øł¾ŻĒśĻßĶ¼»Ų“šĻĀĮŠĪŹĢā£®
ČēĶ¼ŹĒX”¢Y”¢ZČżÖÖ¹ĢĢåĪļÖŹµÄČܽā¶ČĒśĻßĶ¼£¬øł¾ŻĒśĻßĶ¼»Ų“šĻĀĮŠĪŹĢā£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 °ŃŹ¢ÓŠ5g 16%µÄNaOHČÜŅŗµÄ¶ĢŹŌ¹Ü·ÅČėŹ¢ÓŠ10g 16%µÄCuSO4ČÜŅŗµÄ׶ŠĪĘæĄļ£¬ČēĶ¼ĖłŹ¾£¬Ē抱׶ŠĪĘæÖ±µ½Ź¹Į½ČÜŅŗ³ä·Ö»ģŗĻ£¬»ģŗĻŗó²»æÉÄܵďĒ£Ø””””£©
°ŃŹ¢ÓŠ5g 16%µÄNaOHČÜŅŗµÄ¶ĢŹŌ¹Ü·ÅČėŹ¢ÓŠ10g 16%µÄCuSO4ČÜŅŗµÄ׶ŠĪĘæĄļ£¬ČēĶ¼ĖłŹ¾£¬Ē抱׶ŠĪĘæÖ±µ½Ź¹Į½ČÜŅŗ³ä·Ö»ģŗĻ£¬»ģŗĻŗó²»æÉÄܵďĒ£Ø””””£©| A£® | ²śÉśĄ¶É«³Įµķ0.98g | |
| B£® | ׶ŠĪĘæÄŚĪļÖŹ×ÜÖŹĮæ²»±ä | |
| C£® | ĖłµĆČÜŅŗµÄNa2SO4ÖŹĮæ·ÖŹż“óÓŚ9.5% | |
| D£® | ĖłµĆµÄNa2SO4ČÜŅŗÖŹĮæÓėŌCuSO4ČÜŅŗÖŹĮæĻąµČ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com