
(10分)在做“铁在氧气里燃烧”实验时,小芳等同学进行了以下探究活动,请你一同参与。
【探究一】探究铁丝燃烧是否需要纯氧
【实验内容】取0.38mm的铁丝,分别在体积分数为90%、70%、65%、60%、55%的氧气中进行实验。
实验现象
|
O2% |
90% |
70% |
65% |
60% |
55% |
|
实验现象 |
燃烧剧烈、燃烧时间长,效果好 |
燃烧比90%弱,燃烧时间短,实验成功 |
燃烧比70%弱,燃烧时间比70%短,实验成功 |
燃烧比65%弱,燃烧时间更短,实验成功 |
难以燃烧,只是发红 |
【结论】就0.38mm铁丝而言,燃烧所需氧气的最低体积分数为 ,且氧气浓度越大,燃烧现象越 。(填“剧烈”或“不剧烈”);
【拓展】上述关于铁丝燃烧所需氧气最低浓度的结论是否合理,请说出理由?
(填 “合理”或 “不合理”),理由: ;
【探究二】探究铁丝燃烧产生火星四射的原因
【实验内容】:取纯铁丝和铁丝含碳量分别为0.1%、0.32%、0.52%、0.69%的铁丝 (直径均为0.20mm),分别在氧气中进行实验。
|
C % |
纯铁丝 |
0.1% |
0.32% |
0.52% |
0.69% |
|
实验现象 |
无火星四射现象,熔断 |
有短暂火星四射现象,实验欠成功 |
火星四射现象明显,实验成功 |
燃烧比0.32%剧烈,火星四射更明显,实验成功 |
燃烧比0.52%更剧烈,火星四射,实验成功 |
【结论】:铁丝燃烧产生火星四射现象和 (填元素符号)有关,就0.20mm铁丝而言,燃烧剧烈程度和其含量的关系为 。
【探究三】:探究铁丝的纯度
探究小组取2.10g 铁丝在足量的氧气中充分燃烧,产物经过除杂处理后,得到四氧化三铁的质量为2.32g,试通过计算求出铁丝中铁的质量分数。(要求写出计算过程)(4分)
[探究一]: >55% 剧烈 (1)不合理,因为,0.38mm的铁丝可能在氧气浓度为56%~59%的范围内燃烧
[探究二]:C 对0.2mm的铁丝而言,含碳量越高,火星四射现象越明显
[探究三]:解:(1)求出四氧化三铁中的铁的质量1.68g…2分(格式不规范,扣1分)
(2)求出铁的质量分数80%…2分 (格式不规范,扣1分)
【解析】由[探究一]可知,铁丝在55%的O2中不能燃烧,故铁丝燃烧所需氧气浓度最低体积分数要大于55%;且氧气浓度越大,铁丝燃烧的现象就越剧烈。由于 铁丝有可能在氧气浓度为56%~59%的范围内燃烧,故上述结论不合理。
[探究二]对比实验现象可知,铁丝燃烧产生火星四射现象和碳元素有关,对0.2mm的铁丝而言,含碳量越高,火星四射现象越明显。
[探究三]2.32g四氧化三铁中含铁元素的质量为
2.32g×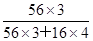 =1.68g
=1.68g
根据质量守恒定律,则说明2.10g铁丝中含铁元素的质量为1.68g,则铁丝中铁的质量分数为
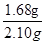 ×100%=80%
×100%=80%
答:该铁丝中铁的质量分数为80%.


科目:初中化学 来源: 题型:
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
科目:初中化学 来源:2010-2011学年山东省日照市莒县九年级(上)期末化学试卷(解析版) 题型:解答题
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
科目:初中化学 来源:2011年天津市东丽区中考化学一模试卷(解析版) 题型:解答题
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
科目:初中化学 来源:2010年江苏省徐州市中考化学试卷(解析版) 题型:解答题
| Fe3O4 | Fe2O3 | 铁 | |
| 分解温度/℃ | 1538 | 1400 | - |
| 熔点/℃ | - | - | 1535 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com