
实验室常用(a)~(e)装置制取和收集气体.
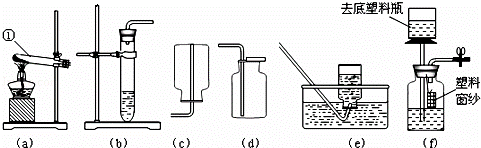
步骤一:选取药品与发生装置.实验室经常选用稀盐酸和 (填药品名称)作为
反应物,发生装置可选用如上图中的 .
步骤二:检查装置气密性.组装好仪器后,将导管末端浸末在水中,用手捂试管,
发现导管口 ,放手后有 ,则气密性良好.
步骤三:反应并收集气体.收集二氧化碳可以用排水法或向上排空气法.到底哪种方法更好,甲、乙两同学分别用排水法和排空气法做如下实验研究(用的药品与发生装置一样)
| 1、比较收集时间:分别收集满一个集气瓶的二氧化碳,记录时间 | 甲:收集时间较短 乙:收集时间较长 | 原因: C (选择填空,下同 ) |
| 2、比较收集到气体的浓度:分别向两个集气瓶中加入两滴管的澄清石灰水 | 甲:石灰水先变浑浊 乙:石灰水后变浑浊 | 原因: A |
A.甲收集到的二氧化碳纯度更高 B.产生气体速度不一样
C.气态分子间隔大,运动速度快,不同气体分子更易混合,不易分离
结论:综上所述, (填收集方法)收集二氧化碳更好.
反思:排水法收集二氧化碳仍有不足之处,请写出一点
[思考]丙同学对发生装置中的废液进行了研究.
(1)测出该废液的pH<7,则废液中存在的阳离子为 .
(2)向此废液滴加碳酸钠溶液至过量,则下列图象表示正确的为 .

(3)小明是一位爱动手做实验的同学,他找来塑料瓶和一些其他用品,制作成如图(f)的装置.图中去底塑料瓶和其相连导管的组合相当于实验室中的 (填一种仪器的名称).该装置作为制取二氧化碳气体发生装置的优点是 .
| 步骤一:实验室制取二氧化碳用稀盐酸和大理石或石灰石;并据反应物的状态和反应条件选择发生装置; 步骤二:据检查装置气密性的方法是利用了气体压强的变化分析解答; 步骤三:运用对比实验来探究排水法和排空气法哪种方法好、运用分子的性质、二氧化碳使澄清的石灰水变浑浊的先后分析解答; 结论:根据步骤三中的探究实验得出结论; 反思:运用排水法收集气体的方法解答; 思考:(1)运用pH<7说明溶液呈酸性,结合碳酸钙和稀盐酸反应生成氯化钙、水、二氧化碳解答; (2)运用碳酸钠和盐酸反应生成二氧化碳、氯化钙和碳酸钠反应产生碳酸钙沉淀解答; (3)据装置特点和常用仪器的用途分析解答. | |
| 解答: | 解:步骤一:实验室运用大理石或石灰石与稀盐酸反应生成二氧化碳,常温下即可反应,大理石或石灰石是固体,盐酸是液体,故发生装置选择b或f; 步骤二:检查装置的气密性用手握住容器外壁,导管口有气泡冒出,导管离开水面后容器内由于气压减小导管中有一段小水柱; 步骤三:根据实验(1)可知:甲:收集时间较短,乙:收集时间较长,说明气态分子间隔大,运动速度快,不同气体分子更易混合,不易分离,所以利用向上排空气法收集的速度慢;由(2)可知:甲:石灰水先变浑浊,乙:石灰水后变浑浊,说明甲收集的二氧化碳纯度更好,乙中可能有混入的少量氯化氢气体,溶于水与部分石灰水反应,所以甲先变浑浊; 结论:由步骤三可得出运用排水法收集的气体较为纯净; 反思:运用排水法收集二氧化碳时水蒸气会混入气体中,不能得到干燥的二氧化碳; 思考:(1)碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳故,溶液中含有钙离子,由题意知溶液的pH<7说明溶液呈酸性,说明盐酸过量,故溶液中含有阳离子﹣﹣氢离子; (2)滴加碳酸钠先和溶液中的酸反应,溶液的pH增大,再和溶液中的氯化钙反应生成碳酸钙沉淀和氯化钠在这一过程中溶液的pH不变等于7,氯化钙全参加反应后再加碳酸钠溶液的pH会大于7且增大,所以图象B正确; (3)观察图示可知去底塑料瓶和其相连导管的组合相当于实验室中的长颈漏斗用途相似;利用该装置的优点在于可以随时添加药品,且可通过弹簧夹的开闭控制反应的发生和停止; 故答案为:步骤一:大理石或石灰石; b或f; 步骤二:有气泡; 导管中有一小段水柱; 步骤三:C;A; 结论:排水法; 反思:混有少量水蒸气或得不到干燥的二氧化碳(答案合理均可); 思考:(1)Ca2+、H+; (2)B; (3)长颈漏斗,可随时添加药品、可控制反应的开始和结束(答案合理均可). |


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| △ |
| ||
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com