
| 相对原子质量×原子个数 |
| 相对分子质量 |
| 14×2 |
| 14×2+1×4+16×3 |
| 170 |
| x |
| 58.5 |
| y |
| 143.5 |
| 14.35g |
| 17g |
| 170g |


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源: 题型:
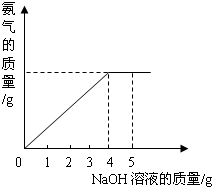 硝酸铵是农业生产中常用的化学肥料.为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取 2.0g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH溶液.发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O.反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:
硝酸铵是农业生产中常用的化学肥料.为测定某含有少量NaNO3的硝酸铵样品中NH4NO3的纯度,取 2.0g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH溶液.发生如下反应:NH4NO3+NaOH=NaNO3+NH3↑+H2O.反应过程中放出的氨气质量及加入的NaOH溶液的质量的关系如图所示:查看答案和解析>>
科目:初中化学 来源: 题型:
| ××××牌 优质硝铵 (NH4NO3) 含氮量高达40.1%(1)NH4NO3中氮、氢、氧三种元素的质量比; (2)通过计算硝酸铵的含氮量(氮元素的质量分数),说明此标签是否有错误; (3)求1 00kg硝酸铵(NH4NO3)中含氮元素质量是多少? 查看答案和解析>> 科目:初中化学 来源: 题型: 在某公共场所,有如下广告:
|