
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO2)2 |
| 颜色 | 白色 | 白色 | 淡黄色 | 白色 |
| 实验操作 | 实验现象 | 实验结论和化学方程式 |
| 将点燃的镁条伸入充满氮气的集气瓶中燃烧,观察现象 | 生成淡黄色的固体 | 小茜的猜想成立,化学方程式为 3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2. |
分析 【查阅资料】:根据质量守恒定律确定产物中一定不存在氯化镁;
【提出猜想】:根据空气的成分和固体的颜色判断淡黄色固体的来源;
【实验探究】:根据在纯氧气中燃烧镁条只生成白色固体,在纯氮气中燃烧镁条只生成淡黄色色固体,可采取在纯纯氮气中燃烧镁条,观察现象的方法;得出结论并根据反应的反应物、生成物和反应条件书写方程式;
【拓展运用】:根据Mg在空气中燃烧只考虑与氮气和氧气反应的情况.
解答 解:【查阅资料】:根据质量守恒定律,化学反应前后元素的种类不变,由于空气中无氯元素,所以燃烧产物中一定不存在氯化镁;
【提出猜想】:空气中含有氮气,在空气中点燃镁条时,生成的白色固体物质中夹杂着少量的淡黄色固体,而氮化镁为淡黄色,所以淡黄色的固体可能是镁与空气中的氮气反应生成的;
【实验探究】由于在纯氧气中燃烧镁条只生成白色固体氧化镁,在纯氮气中燃烧镁条只生成淡黄色色固体氮化镁,可用在纯氮气中燃烧镁条,观察现象的方法;镁和氧气在点燃的条件下燃烧生成氧化镁,化学方程式为:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;镁和氮气在点燃的条件下反应生成氮化镁,化学方程式:3Mg+N2 $\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
【拓展运用】
设72g镁与空气中的氮气完全燃烧生成物的质量为x
3Mg+N2 $\frac{\underline{\;点燃\;}}{\;}$Mg3N2
72 100
72g x
$\frac{72}{72g}$=$\frac{100}{x}$
x=100g
设72g镁与空气中的氧气完全燃烧生成物的质量为y
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
48 80
72g y
$\frac{48}{72g}$=$\frac{80}{y}$
y=120g
故72g镁在空气中完全燃烧,所得含镁产物的总质量范围是100g~120g.
故答案为:(1)空气中无氯元素;
(2)N2;
(3)
| 将点燃的镁条伸入充满氮气的集气瓶中燃烧,观察现象 | 生成淡黄色的固体 | 小茜的猜想成立,化学方程式为 3Mg+N2═Mg3N2. |
点评 正确理解质量守恒定律的内容,了解燃烧的定义及定义的拓展意义是解决问题的关键,书写化学方程式一定要确定反应物和生成物的化学式,不要忘记配平和条件,并能根据方程式计算.


 优生乐园系列答案
优生乐园系列答案科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
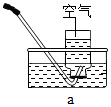 我市某中学曹老师带领学生进行有关的氧气实验时,发现“一同学不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃”;对此,曹老师让该同学往集气瓶装入半瓶水,再用排水法收集$\frac{1}{2}$集气瓶的氧气,发现瓶中的氧气也能使带火星木条复燃.收集装置如图,空气中氧气的体积分数约为21%.计算本实验中,集气瓶内的氧气含量实际为多少?(写出计算过程,结果保留一位小数).
我市某中学曹老师带领学生进行有关的氧气实验时,发现“一同学不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃”;对此,曹老师让该同学往集气瓶装入半瓶水,再用排水法收集$\frac{1}{2}$集气瓶的氧气,发现瓶中的氧气也能使带火星木条复燃.收集装置如图,空气中氧气的体积分数约为21%.计算本实验中,集气瓶内的氧气含量实际为多少?(写出计算过程,结果保留一位小数).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
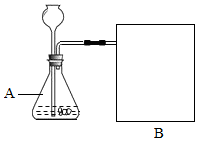 研究性学习小组选择“过氧化氢(H2O2)溶液生成氧气(O2)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
研究性学习小组选择“过氧化氢(H2O2)溶液生成氧气(O2)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:| 实验编号 | 1 | 2 |
| 反应物 | 6%过氧化氢溶液 | 6%过氧化氢溶液 |
| 催化剂 | 1g二氧化锰 | 1g红砖粉 |
| 时间 | 35s | 152s |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 催化剂改变了反应速率 | B. | 反应物与生成物均有分子构成 | ||
| C. | 生成物之一为C2H2 | D. | 反应前后原子的种类发生了变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
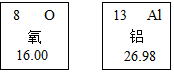
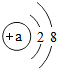
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com