
| A. | 闻气味 | B. | 将集气瓶倒扣在水中观察 | ||
| C. | 观察颜色 | D. | 用带火星的木条伸入到集气瓶中 |
分析 鉴别空气、氧气两瓶气体,要求根据两种气体性质的不同,设计的方案能出现两种明显不同的实验现象,才能达到达到一次鉴别出两瓶气体的目的.
解答 解:A、空气、氧气均没有气味,用闻气味的方法无法鉴别,故选项错误.
B、由于氧气不易溶于水,而空气中主要含有氮气和氧气,氮气难溶于水,将集气瓶倒扣在水中观察,均无明显现象,不能鉴别,故选项错误.
C、空气、氧气均没有颜色,用观察颜色的方法无法鉴别,故选项错误.
D、氧气能支持燃烧,带火星木条伸入氧气中,能使其复燃,空气中无明显现象,可以鉴别,故选项正确.
故选:D.
点评 本题考查了常见气体的鉴别方法,解题的关键是利用所要鉴别气体的性质的差别,根据实验中是否出现明显的不同现象判断能否鉴别.


 智慧小复习系列答案
智慧小复习系列答案科目:初中化学 来源: 题型:解答题
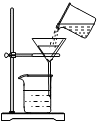 阅读下列材料,回答问题
阅读下列材料,回答问题查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 小奋同学发现他家菜园中的蔬菜生长迟缓,便到庄稼医院买回了一包氮肥(主要成分是硝酸铵NH4NO3),如图是这包氮肥包装标签上的部分文字.试计算:
小奋同学发现他家菜园中的蔬菜生长迟缓,便到庄稼医院买回了一包氮肥(主要成分是硝酸铵NH4NO3),如图是这包氮肥包装标签上的部分文字.试计算:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
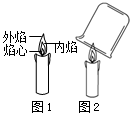 小华同学在准备“对蜡烛及其燃烧的探究活动”时,发现实验室有许多用剩下的小蜡烛头,感觉浪费了太可惜.于是带领实验小组的同学用小蜡烛头为原料制造蜡烛.其过程如下:
小华同学在准备“对蜡烛及其燃烧的探究活动”时,发现实验室有许多用剩下的小蜡烛头,感觉浪费了太可惜.于是带领实验小组的同学用小蜡烛头为原料制造蜡烛.其过程如下:
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
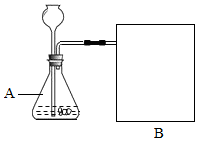 研究性学习小组选择“过氧化氢(H2O2)溶液生成氧气(O2)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
研究性学习小组选择“过氧化氢(H2O2)溶液生成氧气(O2)的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:| 实验编号 | 1 | 2 |
| 反应物 | 6%过氧化氢溶液 | 6%过氧化氢溶液 |
| 催化剂 | 1g二氧化锰 | 1g红砖粉 |
| 时间 | 35s | 152s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com