
分析 根据化合物中各元素化合价代数和为零,计算物质中某元素的化合价;提取有用信息得出物质性质差异而进行除杂的操作设计.
解答 解:根据化合物中各元素化合价代数和为零,在NH4Cl中,Cl是-1价,H是+1价,设N的化合价为x,则x+(+1)×4+(-1)×1═0 解之得 x=-3;
根据反应2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑可知:NaHCO3受热易分解生成纯碱、二氧化碳和水,因此,除去混在Na2CO3粉末中少量的NaHCO3的方法为加热分解NaHCO3;
①NH3+CO2+H2O═NH4HCO3属于化合反应,②NH4HCO3+NaCl═NH4Cl+NaHCO3属于复分解反应,③2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$2Na2CO3+H2O+CO2↑属于分解反应.
故填:-3;加热;三.
点评 本题考查质量守恒定律、元素化合价和提取有用信息得出物质性质差异而进行除杂.


 学习实践园地系列答案
学习实践园地系列答案科目:初中化学 来源: 题型:解答题
| 青蒿素含量(mg/g) | ||||
| 第1次 | 第2次 | 第3次 | ||
| 根 | 1.02 | 1.05 | 1.14 | |
| 茎 | 0.09 | 0.11 | 0.10 | |
| 叶(叶龄7天) | 4.57 | 4.65 | 4.58 | |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
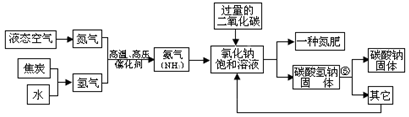
| A. | 该流程的原料有空气、焦炭、水、氯化钠等物质 | |
| B. | 该流程除了制得产品纯碱之外,还能制得氮肥氯化铵 | |
| C. | 该流程中使用氯化钠的饱和溶液,有利于碳酸氢钠固体的析出 | |
| D. | 该流程中“其它”指示可循环利用的物质有二氧化碳、水两种物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
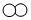 ”和“
”和“ ”代表两种不同的物质分子,它们在一定条件下能发生化学反应,反应前后的微观模型如下图所示,下列说法正确的是( )
”代表两种不同的物质分子,它们在一定条件下能发生化学反应,反应前后的微观模型如下图所示,下列说法正确的是( )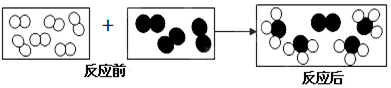
| A. | 参加反应的“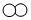 ”和“ ”和“ ”分子的个数比是2:1 ”分子的个数比是2:1 | |
| B. | 该反应有2种生成物 | |
| C. | 该反应是化合反应 | |
| D. | 每个生成物分子由3个原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 该反应不符合复分解反应发生的条件 | |
| B. | 该反应中四种物质都是盐 | |
| C. | 反应后可用过滤的方法分离出NaHCO3 | |
| D. | 反应后的溶液中不能继续溶解NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
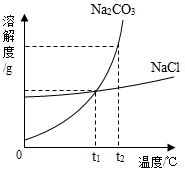 1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl ②2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑试回答下列问题:
1926年,我国著名化学家侯德榜先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①NaCl+NH3+CO2+H2O=NaHCO3+NH4Cl ②2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com