
 (1)实验室制取氧气反应的化学方程式为
(1)实验室制取氧气反应的化学方程式为
| ||
| ||
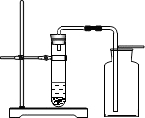 或
或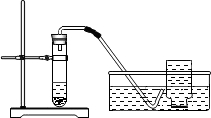


科目:初中化学 来源: 题型:
| A、水分子体积增大了 |
| B、水分子发生了分裂 |
| C、水分子的数目增多了 |
| D、水分子之间的间隔变大了 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、木炭在氧气中燃烧,发出红光,生成黑色固体 |
| B、铝箔在氧气中燃烧,发出白光,生成白色固体 |
| C、红磷在氧气中燃烧,产生大量白雾 |
| D、硫在氧气中燃烧,发出微弱的淡蓝色火焰 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、7.6g | B、15.2g |
| C、20.0g | D、40.0g |
查看答案和解析>>
科目:初中化学 来源: 题型:
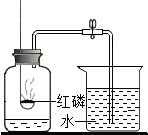 测定空气中氧气含量的实验装置如图所示.
测定空气中氧气含量的实验装置如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:
| A、溶液中溶质的质量保持不变 |
| B、溶液中溶质的质量分数始终为a% |
| C、溶液中溶质的质量分数开始增大后又逐渐减小到a% |
| D、溶液中溶质的质量分数开始减小后又逐渐增大到a% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com