
【题目】钠是人体必需的常量元素,人体中含钠 80~120g,对于维持人体内的水分和维持体液恒定的 pH起重要的作用。如图是钠在元素周期表中的相关信息,下列说法正确的是
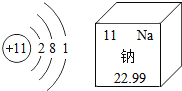
A.钠原子核内有 11 个中子B.钠原子的质量为 22.99g
C.钠在化学反应中易失去电子D.金属钠中钠元素的化合价为+1
科目:初中化学 来源: 题型:
【题目】(1) 为庆祝中国人民海军成立70周年,2019年4月23日在青岛海域举行了海上阅兵活动。70年来人民海军在党的坚强领导下,一路劈波斩浪,纵横万里海疆,取得举世瞩目的伟大成就,正以全新资态屹立于世界的东方!中方参阅舰艇和飞机包括航母辽宁舰、新型核潜艇、新型驱逐舰、战机等在内,有些舰艇是第一次亮相。

①军舰外壳需要涂防锈漆,目的是为了防止铁与空气中的_____发生反应而生锈。
②核潜艇上一般备有的氧气再生药板,是由一片片涂有过氧化钠(Na2O2)的薄板组成,使用时过氧化钠与二氧化碳反应生成氧气和碳酸钠,请写出该反应的化学方程式_____。
(2)工业上采用氨碱法生产纯碱(Na2CO3) ,主要流程如图:
![]()
其生产过程中有下列反应:①![]() ;②
;②![]() ;碳酸氢钠和氯化铵的溶解度曲线如图所示。
;碳酸氢钠和氯化铵的溶解度曲线如图所示。
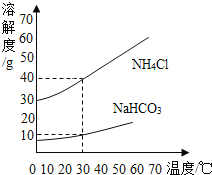
请回答下列问题:
①30℃时, NH4Cl饱和溶液的溶质质量分数_____NaHCO3饱和溶液的溶质质量分数(填“大于”“小于”“等于”之一)。
②30℃时,将25gNH4Cl加入到50g水中,所得溶液的溶质质量分数为_____(计算结果精确到0.1%)。
③氨盐水吸收二氧化碳后生成碳酸氢钠和氯化铵,碳酸氢钠首先结晶析出,请根据它们的溶解度曲线,从溶解度角度分析原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体时需要的一些装置如下图所示,请回答下列问题:

(1)写出标有序号的仪器名称:①____。
(2)实验室制取氧气和二氧化碳的发生装置都可选用B装置的原因是__。
(3)若要得到干燥的氧气,所选择装置的连接顺序为: B→__(填字母序号);
(4) F装置可用于气体的收集、检验、除杂等,用该装置能完成的实验是___(填字母序号)。
A 排空气法收集氢气时,气体从b端通入,收集氢气
B 瓶内装满水,氧气从a端通入,收集氧气
C 瓶内装有澄清石灰水,气体从a端通入,检验氧气中是否混有二氧化碳
D 瓶内裝有浓硫酸,气体从b端通入,吸收氢气中混有的水蒸气
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面的科普材料。
浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还蕴藏着丰饶的矿产;而海水本身含有大量的化学物质,又是宝贵的化学资源。海水中含有多种盐类,如氯化钠、氯化镁、硫酸钙等。
利用海水制盐的方法在我国仍以蒸发法为主,它的原理很简单,即在太阳照射后,海水受热使水分蒸发,当各种盐分别达到其饱和浓度时,依次以固态形式析出。随着科学和技术的进步,人们还利用其他方法从海水中制盐,如电渗析法、冷冻法等,用这两种方法不但可以制盐,同时也可以得到淡水。
食盐不仅是人类生活所不可缺少的物质,还是一种重要的化工原料。例如,作为基本化学工业之一的氯碱工业,就是通过电解饱和食盐水的方法得到氢氧化钠、氯气和氢气,并进而生产盐酸、漂白粉、塑料、肥皂和农药等,其他如造纸、纺织、印染、有机合成和金属冶炼等,也都离不开由食盐制得的化工产品。
海水可以提取食盐,还是个巨大的资源宝库。可以得到溴、镁等物质。目前,从海水中提取的溴约占世界溴年产量的三分之一。常用的技术叫做吹出法,即用氯气与溴化钠在酸性条件下反应,使其转变为溴后,用空气将其吹出。也可以用水蒸气,使溴和水蒸气一起蒸出。
而海水中的镁,则更是一种重要的资源。工业规模海水提镁的方法,是将海水抽入反应槽中,加入石灰乳,将海水中的镁转变为沉淀;再加入稀盐酸转化为氯化镁溶液,过滤、烘干,然后电解熔融状态的氯化镁就得到镁和氯气;氯气可以用来制取盐酸,再循环使用。
从海水得到的粗盐中含有泥沙、氯化钙、氯化镁、硫酸钠等杂质,用于电解法制碱必须经过精制。精制食盐水常加入一些试剂,使杂质沉淀过滤出来,再加入稀盐酸调节盐水的pH。
回答下列问题:
(1)根据材料可知,从海水中提取溴常用的技术叫做_______。
(2)铝和镁一样,属于活泼金属,铝在常温下具有较强抗腐蚀性的原因是_______。
(3)如果加入稀盐酸后盐水的pH=7,则溶液显_______性。
(4)根据材料可知,电解饱和食盐水的化学方程式为_______。
(5)要除去粗盐中含有的Na2SO4、MgCl2、CaCl2等可溶性杂质,可加入氢氧化钠溶液、碳酸钠溶液。其中,加入氢氧化钠溶液是为了除去_____; 在除去上述杂质时,应该先除去,________(选填“Na2SO4”或“CaCl2”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业制取硝酸的流程如下:

(1)步骤①反应属于分解反应,其微观实质是_____ ; 步骤②是利用液态氮与液态氧的_____不同。
(2)步骤③中催化剂所起的作用是_____,相应的化学方程式为_____。
(3)步骤④的化学方程式是![]() ,则X的化学式为_____。
,则X的化学式为_____。
(4)流程中循环使用的物质是_____ (写化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组的同学在完成了“用铁和硫酸铜溶液反应来验证质量守恒定律”的实验后, 收集到一桶蓝绿色的废液,经分析可知废液中含有 FeSO4、CuSO4,他们想从中回收金属铜和硫酸 亚铁晶体,设计了如下实验方案。结合实验方案回答下列问题:
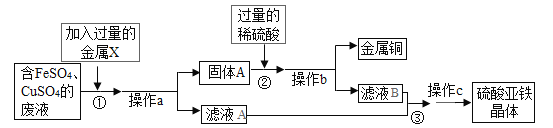
(1)操作 a 的名称是______,该操作中玻璃棒的作用是_____。步骤①中发生反应的化学方程式为_____;
(2)步骤②中加入过量稀硫酸的目的是_____;
(3)从滤液中获得硫酸亚铁晶体采用的方法是_____,对所得晶体,再用少量低温的水洗涤 3次。洗涤用的水必须少量且低温,其原因是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】科技节活动中,化学实验小组做了如下实验,请回答以下问题。
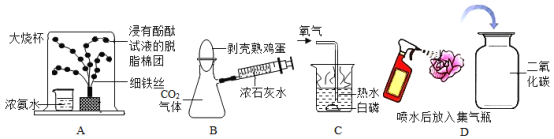
(1)图A所示实验可观察到“铁树”上浸有无色酚酞试液的棉团由白色变为________色,该实验中没有涉及的性质是____________(填字母)。
A氨分子是不断运动的 B氨分子有一定质量 C浓氨水具有挥发性
(2)图B所示实验,将注射器中浓石灰水注入瓶中,会看到鸡蛋被“吞”入瓶中,该实验中涉及的化学方程式为_____________。
(3)图C所示实验,当通过导管向热水中通入氧气时,白磷在水下燃烧,该实验说明燃烧需要的条件为:①可燃物;②达到燃烧所需要的_____________;③__________________。
(4)图D所示实验观察到紫色小花变为红色,小花变红的原因是______________(用化学方程式表示)。
(综合应用)“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻着火,钾遇水生成H2和KOH,其反应化学方程式为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的是
A.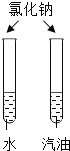 探究同种物质在不同溶剂中的溶解性
探究同种物质在不同溶剂中的溶解性
B.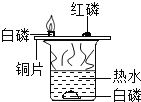 探究物质燃烧的条件
探究物质燃烧的条件
C.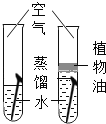 探究铁生锈的条件
探究铁生锈的条件
D.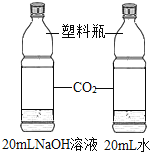 探究
探究![]() 与NaOH溶液能否发生反应
与NaOH溶液能否发生反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图像分别对应四个变化,其中正确的是()
A. 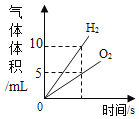 将水通电一段时间
将水通电一段时间
B.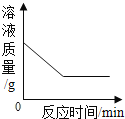 向一定量的硝酸银溶液中插入铜丝
向一定量的硝酸银溶液中插入铜丝
C. 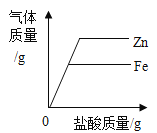 分别向等质量的锌、铁中滴加等质量分数的稀盐酸
分别向等质量的锌、铁中滴加等质量分数的稀盐酸
D. 分别向等质量的溶质质量分数为15%、10%的 盐酸中不断加水
分别向等质量的溶质质量分数为15%、10%的 盐酸中不断加水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com