
| 1 |
| 3 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验序号 | 实验1 | 实验2 | 实验3 |
方案 | 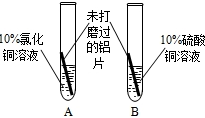 | 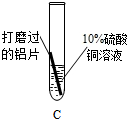 | 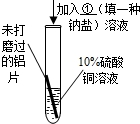 ① |
现象 | A中铝片表面有红色固体析出;B中铝片无明显现象. | 与A中的现象相 | |
结论 | 溶液中对氧化膜产生了破坏作用的离子可能是 | 除去表面氧化膜的铝片会与CuSO4溶液反应.该反应的化学方程式 | 验证了实验1的结论. |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 体重 | 小于等于15千克 | 15~23千克 | 23~40千克 | 大于40千克 |
| 每次用量 | 30mg | 45mg | 60mg | 60mg |
查看答案和解析>>
科目:初中化学 来源: 题型:
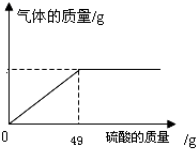 为了分析生铁中铁的含量,某学习小组称取5.9g生铁样品,并粉碎,然后往粉末中逐滴加入质量分数为20%的硫酸,反应过程中产生气体的质量与加入硫酸的质量关系如图所示(假设生铁中杂质不与稀硫酸反应,也不溶于水).
为了分析生铁中铁的含量,某学习小组称取5.9g生铁样品,并粉碎,然后往粉末中逐滴加入质量分数为20%的硫酸,反应过程中产生气体的质量与加入硫酸的质量关系如图所示(假设生铁中杂质不与稀硫酸反应,也不溶于水). 查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
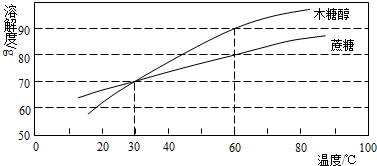
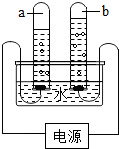 Ⅰ、在农村人们常常饮用河水,河水中常含有大量的泥沙、悬浮物和细菌等杂质,一般可用次氯酸杀死细菌.将漂白粉(主要成分是次氯酸钙)溶于水可生成氯化钙和次氯酸.下列是某户居民在饮用水之前对河水的处理步骤:
Ⅰ、在农村人们常常饮用河水,河水中常含有大量的泥沙、悬浮物和细菌等杂质,一般可用次氯酸杀死细菌.将漂白粉(主要成分是次氯酸钙)溶于水可生成氯化钙和次氯酸.下列是某户居民在饮用水之前对河水的处理步骤:查看答案和解析>>
科目:初中化学 来源: 题型:
| A、NaNO3 KCl CuSO4 |
| B、K2CO3 CaCl2 ZnSO4 |
| C、Fe(NO3)3 NaCl BaCl2 |
| D、NaOH Mg(NO3)2 FeCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com