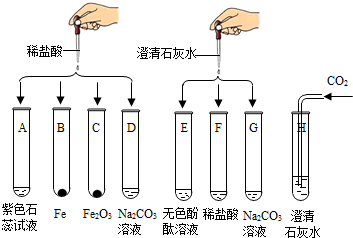
18、请你参与下列探究:
【问题情景】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.这一现象激发起同学们的探究欲望,生成的是什么气体?
【提出猜想】从物质组成元素的角度,放出的气体可能是SO
2、O
2、H
2.
【查阅资料】SO
2易溶于水,它能与NaOH反应,生成Na
2SO
3.
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O
2,则检验方法是
用带火星的木条试验,看木条是否复燃
.
(2)乙同学认为是SO
2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量.写出SO
2与NaOH反应的化学方程式
SO2+2NaOH=Na2SO3+H2O
.
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体.
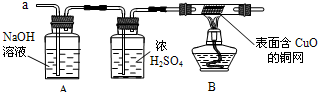
如果放出的是O
2和H
2,你认为方案中的安全隐患是
实验时剩余气体B通过加热的试管易发生爆炸事故
.
丙同学认为:为确保安全,实验前应先收集一试管气体,用拇指
堵住试管囗,靠近火焰点火,
,若不发出
尖锐的爆鸣声
,方可采用上面的装置进行实验.
【实验探究】经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量无增减.
结论:铁粉与硫酸铜溶液反应时,产生的气体是
H2
.
【思维拓展】
(1)由上述实验可以推出,硫酸铜溶液中可能含有
H2SO4
物质.
(2)不通过称量,如何判断SO
2与NaOH溶液发生了反应呢?有一同学设计了右图所示的装置进行实验,发现试管内液面上升,就得出SO
2与NaOH溶液发生反应的结论.其他同学认为这一方案不严谨,理由是
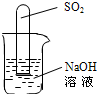
SO2溶于水中也会导致试管内气压减小,液面上升
.要得到科学严谨的结论,仍利用该装置,补做的实验是
把烧杯中的氢氧化钠换成硫酸钠溶液,做一个对比试验
.
CuSO
4溶液对过氧化氢的分解具有催化作用.有同学想猜想其他盐溶液也能在这个反应中起到同样的作用,于是他们做了以下的探究:
(1)清你帮助他们完成实验报告:
| 实验过程 |
实验现象 |
实验结论 |
| 在一支试管中加入5ml5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. |
试管中有大量的气泡产生,伸入的带火星的木条复燃 |
FeCl3溶液可以催化分解H2O2 |
(2)已知FeCl
3在水中可分离出Fe
3+和Cl
-,同学们提出以下猜想:
①甲同学的猜想:真正催化分解H
2O
2的是FeCl
3溶液中的H
2O;
②乙同学的猜想:真正催化分解H
2O
2的是FeCl
3溶液中的Fe
3+;
③丙同学的猜想:真正催华分解 H
2O
2的是FeCl
3溶液中的Cl
-;
你认为最不可能的是
甲
同学的猜想,理由是
因过氧化氢溶液中自身有水,可见水不是催化剂
.
(3)同学们对余下的两个猜想,用实验进行了探究.请你仔细分析后填表:
| 实验过程 |
实验现象 |
实验结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的HCl,并把带火星的木条伸入试管 |
无明显现象 |
起催化作用的不是Cl- |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的 Fe(NO3)3溶液 ,并把带火星的木条伸入试管 |
试管中有大量气泡产生,带火星的木条复燃 |
起催化作用的是Fe3+ |
用18mol/L的硫酸配置100ml 1.0mol/L的稀硫酸,若实验仪器有:
A.100ml量筒 B.托盘天平 C.玻璃棒 D.50ml容量瓶
E.10ml量筒 F.胶头滴管 G.50ml烧杯 H.100ml容量瓶
(1)实验时应选用仪器的先后顺序是(填入编号)
F、E、G、C、H
.
(2)在容量瓶的使用方法中,下列操作不正确的是(填写编号)
B、C、D
.
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配置溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm-2cm处,用滴管滴加蒸馏水到标线.
D.配置溶液时,如果试样是液体,用量筒量取后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1cm-2cm处,用滴管加入蒸馏水到标线.
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次.