
【题目】15%的H2O2溶液在二氧化锰催化作用下会剧烈反应产生O2.实验室欲利用15%的H2O2溶液制取O2,则下列装置中,仪器选择和药品放置最合理的是( )
A. 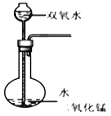 B.
B. 
C.  D.
D. 
科目:初中化学 来源: 题型:
【题目】水是生命活动不可缺少的物质。兴趣小组将浑浊的河水净化,并制成蒸馏水,流程如图1所示。


回答问题:
(1)明矾的作用是_________________,操作Ⅰ是__________ 。
(2)操作Ⅱ:图2装置能除去液体A中的异味和色素,则液体A从b端通入,原因是___________。
(3)操作Ⅲ是_________________。取少量蒸馏水于烧杯中,加肥皂水,搅拌,观察到的现象是_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面的科普短文。
2018年12月,第24届联合国气候大会召开,讨论的核心物质就是CO2。CO2的浓度在过去很长的时间里都保持在一定的范围,随着工业的发展以及化石燃料的大量使用,CO2的排放量不断增加。全球碳循环如图所示:
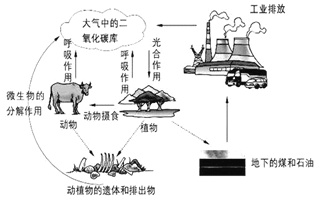

如何降低大气中CO2浓度,是人类一直在研究的重要议题。
海洋封存:利用庞大的水体使海洋成为封存CO2的容器,但会引起海水酸化等。
地质封存:将CO2注入特定的地层,该方法最大的风险是CO2泄漏,局部CO2浓度快速上升,直接威胁人类生命健康等。
矿石碳化:利用矿石中的氧化镁或氧化钙等,在一定条件下与CO2反应,生成碳酸镁或碳酸钙等,但过程缓慢。
综合利用:工业上可以将CO2转化成尿素[CO(NH2)2]、甲醇(CH3OH)等资源。2017年8月,科学家发现了一种镍与有机物组成的混合催化剂,利用太阳光能,将水中溶解的CO2转化成CO和O2。
在二氧化碳的处理过程中,化学起着不可替代的作用。
依据文章内容,回答下列问题。
(1)在全球碳循环中,能消耗二氧化碳的途径是_______。
(2)化石燃料燃烧会产生二氧化碳,因为化石燃料中含有_______元素。
(3)上述综合利用CO2得到的产品中,属于氧化物的是_______。
(4)写出上述将CO2转化成CO和O2的化学方程式_______。
(5)下列说法错误的是_______。
A.碳循环中的“碳”是指碳单质
B.CO2是温室气体,对人类生活有害无利
C.海洋封存CO2会引起海水酸化,发生了反应CO2+H2O ![]() H2CO3
H2CO3
D.矿石碳化过程中,可能发生反应MgO+CO2 MgCO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图一为四种物质的溶解度曲线。如图二所示,分别向试管内滴加一定量的水后,X和Y的饱和溶液均变混浊。
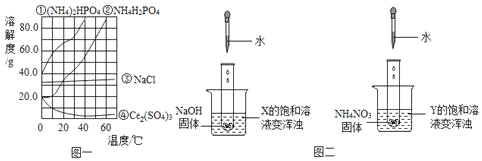
(1)根据图一,10℃时,四种物质溶度从大到小的顺序为_____(填序号)。
(2)根据图二,X对应的图一中的物质是_____(填序号)。
(3)70gNH4H2PO4中混有36g NaCl杂质,可按照以下步骤进行除杂。
①在_____℃下,用100g水行溶解,确保固体刚好完全溶解。
②降温到10℃时,溶液中析出 NH4H2PO4的质量为_____g。
③_____(填操作名称)后,再进行一次溶解及降温结晶,即可得到较纯净的NH4H2PO4。
(4)10℃时,将20g Ce2(SO4)3加入到100g水中,所得溶液的溶质质量分数为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
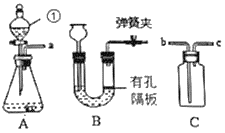
【题目】如图中装置适当组合可用于氧气、氢气、二氧化碳等气体的制备和收集。
(1)仪器①的名称是_____。
(2)若用A装置制取氧气,反应的化学方程式为:_____,该反应属于_____(填基本类型)。
(3)在制取二氧化碳的实验中,装置B与装置A相比,优点是_____。
(4)C装置正放桌面,用于收集A装置中生成的氧气,则a接_____(选填b”或“c”):若将C装满水,用于收集A装置中生成的氢气,则a接_____(选填“b”或“c”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】废旧电路板中主要含有塑料、铜和锡(Sn)等,为实现对其中锡的绿色回收,某工艺流程如下。已知:Sn+SnCl4=2SnCl2 。
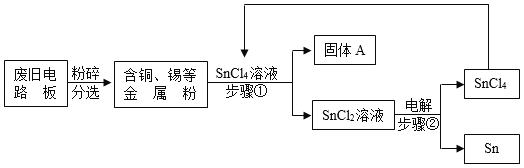
(1)SnCl4中锡元素的化合价是_______________。
(2)铜的金属活动性比锡的________(填“强”或“弱”),固体A中一定含有的金属元素是___________。
(3)写出步骤②发生反应的化学方程式____________,反应的基本类型是______。
(4)相比于直接焚烧废旧电路板回收金属,该工艺主要优点是___________(回答一点即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某些铜制品在空气中久置,表面会生成绿色的铜锈(又称铜绿)。某化学兴趣小组设计并进行如下实验,以探究铜锈的组成和铜生锈的条件。
Ⅰ.探究铜锈的组成
(查阅资料)①铜锈受热易分解 ②硫酸铜粉末遇水由白色变为蓝色
(进行实验)兴趣小组同学从铜器上取下适量的干燥铜锈,按下图所示装置实验(部分夹持装置已略去)。观察到B中白色粉末变为蓝色,C中澄清石灰水变浑浊。
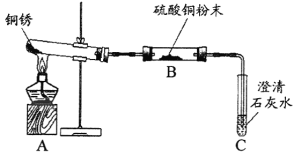
(解释与结论)
(1)C中反应的化学方程式为_________________。
(2)依据以上现象分析,铜锈中一定含有的元素为铜和________(填元素名称)。
Ⅱ.探究铜生锈的条件
(提出猜想)根据铜锈的组成推测,铜生锈可能与CO2、H2O和O2有关。
(进行实验)兴趣小组同学取直径、长度均相同的铜丝,打磨光亮,并设计了如下图所示的5个实验,一周后观察到的实验现象如下表:
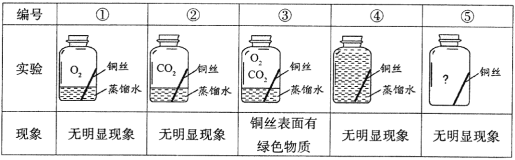
(解释与结论)
(3)实验中都使用了经煮沸并迅速冷却的蒸馏水,“煮沸并迅速冷却”的目的是_____________。
(4)得出“铜生锈一定与CO2有关”的结论,依据的两个实验是___________(填编号)。
(5)对比实验②和③,得出的结论是_____________。
(6)为验证猜想,请在图中将实验⑤补充完整_____________。
(7)由上述实验可推知,铜生锈的条件是_____________。
(反思与应用)
(8)结合上述实验,你对日常生活中保存铜制品的建议是_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】完全电解a g水,在负极上得到20 mL气体,则在正极上得到气体的质量和体积分别是
A. a g,10 mL B. ![]() a g,10 mL C.
a g,10 mL C. ![]() a g,1 0 mL D.
a g,1 0 mL D. ![]() a g,5 mL
a g,5 mL
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是氯元素的原子结构示意图,下列叙述正确的是
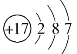
A. 氯原子第一电子层7个电子
B. 氯原子在化学反应中容易失去电子
C. 氯原子核内有17个质子
D. 氯与铝形成物质的化学式为 AlCl2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com