
分析 (1)根据硬水和软水的鉴别方法进行分析;根据硬水软化的方法进行分析;
(2)根据氯化钠的溶解度受温度的影响不大进行分析;
(3)根据饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}$×100%,进行分析解答.
解答 解:(1)生活中可以用肥皂水区分硬水和软水,可以通过加热煮沸的方法降低水的硬度.
(2)氯化钠的溶解度受温度的影响变化不大,海水中含有大量的氯化钠,可以通过蒸发溶剂的方法获得粗盐;
(3)已知20℃时氯化钠的溶解度是36g,设20℃时,100g氯化钠饱和溶液中溶质的质量为x,则$\frac{36g}{36g+100g}=\frac{x}{100g}$,x≈26.47g,可知用30g氯化钠配制100g氯化钠溶液时,则溶质有剩余,此时获得的溶液浓度为氯化钠饱和溶液中溶质质量分数,此时溶液的浓度为:$\frac{26.47g}{100g}×100%=26.47%$;
故答案为:(1)肥皂水;加热煮沸;(2)晾晒海水;(3)26.47%.
点评 本题考查注重基础,比较简单,掌握相关知识即可正确解答,同时通过解答了解了化学知识在生活中的应用,有助于培养学生学习化学的兴趣.


科目:初中化学 来源: 题型:解答题
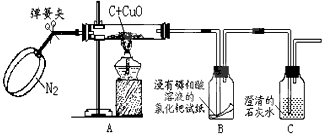 在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”
在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”查看答案和解析>>
科目:初中化学 来源: 题型:解答题
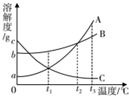 如图为A、B、C三种固体物质的溶解度曲线.
如图为A、B、C三种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
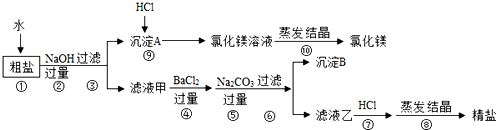
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
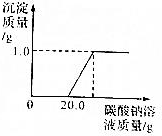
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
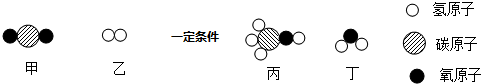
| A. | 该反应是置换反应 | |
| B. | 反应前后分子总数不变 | |
| C. | 发生反应的甲和乙的质量比为22:3 | |
| D. | 反应前后各元素的化合价不发生变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com