
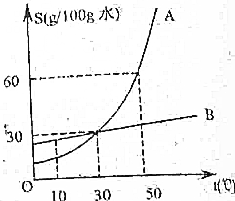
 如图是A、B两种固体的溶解度曲线,请回答下列问题
如图是A、B两种固体的溶解度曲线,请回答下列问题分析 根据固体物质的溶解度曲线可知:①查出某固体物质在某温度下的溶解度,②比较不同的物质在同一温度下的溶解度的大小;③判断物质的溶解度随温度变化的变化情况,进一步确定通过降温还是蒸发溶剂的方法达到结晶的目的等;④固体的溶解度是指在一定的温度下,某固体物质在100克溶剂中达到饱和状态时所溶解的质量.
解答 解:(1)10℃时,A的溶解度小于B的溶解度;故填:<;
(2)30℃时,B的溶解度为30g;故填:30;
(3)A、B的溶解度都随随温度的升高而增大,但A的溶解度受温度的影响较大,故可采用降温结晶的方法提纯;故填:降温结晶;
(4)50℃时,A的溶解度为60g,100g水中最多能溶解60gA物质,设恰好完全溶解120g A形成饱和溶液需要水的质量为x,即120g:x=160g:100g x=75g;故填:75;
(5)50℃时,A物质的溶解度为60g,也就是在该温度下的100g水中最多能溶解60gA物质,那么该温度下的50g水中最多能溶解30gA物质,则该温度下,20克A物质放入50克水中,完全溶解,形成了70g不饱和溶液,可通过加溶质或蒸发溶剂的方法使之转化为饱和溶液;故填:70;不饱和溶液;加溶质(或蒸发溶剂);
(6)30℃时,B物质的溶解度为30g,也就是该温度下,100g水中最多能溶解30gA物质就达到饱和,则该温度下50g水中最多能溶解15gB物质,则将20gB物质溶解在50g水中,只能溶解15g,还有20g-15g=5g晶体没有溶解;故填:5;
(7)A物质的溶解度随着温度的升高而增大,随着温度的降低而减小,所以将50℃的A饱和溶液降温至20℃,会有晶体析出,溶质的质量会减小,溶剂的质量不变,溶液的质量也是减少;因为有晶体析出,所以为20℃时A物质的饱和溶液;故填:溶剂;是;
(8)A物质在50℃时的溶解度比B物质大,且A物质的溶解度受温度的影响比B要大得多,所以50℃时,A和B的饱和溶液,降低温度析出晶体较多的是A;故填:A.
点评 本题考查的是溶解度曲线的应用,完成此题,可以依据已有的溶解度曲线的意义进行解答.


科目:初中化学 来源: 题型:选择题
| A. | 青蒿素属于氧化物 | |
| B. | 青蒿素中碳、氢、氧元素质量比为15:22:5 | |
| C. | 青蒿素由C、H、O 三种元素组成 | |
| D. | 青蒿素是由15 个碳原子、22 个氢原子和5 个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | FeO | B. | Fe2O 3 | C. | Fe3O4 | D. | FeO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 它的相对分子质量是64g | B. | 它是由两个氧分子构成 | ||
| C. | 它是氧元素组成的另一种单质 | D. | 它是一种新型的化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com