
| A. | CH4、H2 | B. | CH4、CO | C. | CO、H2 | D. | CH4、CO2 |
科目:初中化学 来源: 题型:选择题
| A. | 将气体通过灼热的氧化铜 | B. | 将气体通入足量的澄清石灰水中 | ||
| C. | 将气体点燃 | D. | 倾倒,将上层的二氧化碳倒出 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
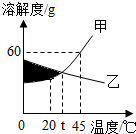 如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )| A. | 甲物质的溶解度为60g | |
| B. | 阴影部分各点对应的溶液(不包括曲线上的点)是甲的不饱和溶液,乙的饱和溶液 | |
| C. | 升高温度可使不饱和的甲溶液变为饱和 | |
| D. | 45℃时,两物质各10克分别加水至恰好溶解,所得饱和溶液质量是甲小于乙 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 有少量气泡 木条不复燃 | 常温下过氧化氢溶液分解速率很慢. | |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 产生大量的气泡 木条复燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com