

分析 (1)依据金属的用途和性质加以分析;
(2)根据金属的活动性,化学方程式的书写方法,进行分析;
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式;根据化合物中正负化合价代数和为零进行分析;
(4)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,要验证铜、铁、银三种金属的活动性强弱,可以从金属与酸的反应或与盐溶液的反应着手分析.
解答 解:(1)A.铁锅是主要利用铁的导热性;B.铜导线主要利用铜的导电性;C.铝箔主要利用铝的延展性,D.银币利用其化学性质稳定.
(2)根据金属的活动性,可知:铝>铁>铜>银,故所给四种金属中活动性最强铝与稀盐酸反应生成氯化铝和氢气,反应的化学方程式为:2Al+6HCl═2AlCl3+3H2↑.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式Cu+2H2SO4═CuSO4+X↑+2H2O,反应前铜、氢、硫、氧原子个数分别为1、4、2、8,反应后的生成物中铜、氢、硫、氧原子个数分别为1、4、1、6,根据反应前后原子种类、数目不变,则每个X分子由1个硫原子和2个氧原子构成,则物质X的化学式为SO2;
因为铜元素显+2价,氧元素显-2价,则设硫酸铜中硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+2)+x+(-2)×4=0,则y=+6价,故CuSO4中的硫元素的化合价为+6价.
(4)A、因铁与Cu(NO3)2溶液发生金属之间的置换反应,则金属的活泼性铁>铜,而银不与Cu(NO3)2溶液反应,则金属的活泼性铜>银,则可一次验证,故A正确;
B、三种金属都不能与Fe(NO3)2溶液反应,无法验证三种金属的活动性顺序,故B错误;
C、铁和铜都能与硝酸银溶液反应,无法验证铁和铜的活泼性强弱,故C错误;
D、铜和银都不与稀硫酸反应,无法验证金属铜与银的活泼性强弱,故D错误;
故选A.
故答案为:
(1)B; 稳定.(2)2Al+6HCl═2AlCl3+3H2↑.(3)SO2,+6.(4)A.
点评 此题考查各种金属的物理性质和金属活动性顺序表.此题很简单,已在考察基础知识的运用.学生应熟悉物质的性质及物质之间的反应来解答.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
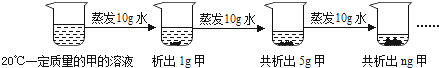
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 37.2g | B. | 18.6g | C. | 9.3g | D. | 无法计算 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
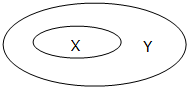 小潘同学按照如图特点对知识进行了归纳,其中匹配的是( )
小潘同学按照如图特点对知识进行了归纳,其中匹配的是( )| A | B | C | D | |
| X | 碳酸钙 | 塑料 | 酒精 | 泥浆 |
| Y | 有机物 | 合成材料 | 化石燃料 | 溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com