
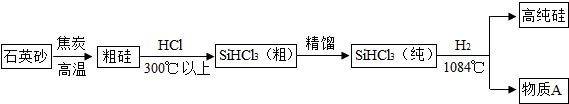
分析 (1)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物R的化学式;由反应特征确定反应类型.
(2)根据混入O2,还原出的Si会被再次氧化,得不到高纯硅;可燃气体与空气或氧气混合达到爆炸极限,遇到明火,会发爆炸,进行分析解答.
(3)根据既是反应物,也是生成物的物质,可以循环使用进行分析解答.
解答 解:(1)由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2R,反应前硅、氧、碳原子个数分别为1、2、2,反应后的生成物中硅、氧、碳原子个数分别为1、0、0,根据反应前后原子种类、数目不变,则2R分子中含有2个碳原子和2个氧原子,则每个R分子由1个碳原子和1个氧原子构成,则物质X的化学式为CO.
该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的反应,属于置换反应.
(2)在H2还原SiHCl3过程中混入O2,还原出的Si会被再次氧化,得不到高纯硅;氢气具有可燃性,与氧气混合达到爆炸极限时在加热或点燃条件下会发生爆炸,故整个制备过程必须达到无水无氧.
(3)氢气与SiHCl3反应生成高纯硅和A(由质量守恒定律,反应前后元素种类不变,则该物质为氯化氢),该物质既是反应物,也是生成物,可以循环使用,A的化学式是HCl.
故答案为:(1)CO;置换反应;
(2)硅被氧化得不到高纯硅,还会引起爆炸;
(3)HCl.
点评 本题难度不大,理解生产高纯硅的流程图,掌握质量守恒定律、防止爆炸的措施等是正确解答本题的关键.


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
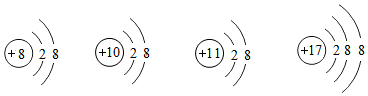
| A. | 它们都带电荷 | B. | 它们都具有相对稳定结构 | ||
| C. | 它们的核外电子排布不完全相同 | D. | 它们属于不同种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜丝用于生产电线 | B. | 在实验室用浓硫酸做干燥剂 | ||
| C. | 葡萄糖给病人补充能量 | D. | 金刚石用来裁玻璃、切割大理石 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com