
| A. | 金属M可能是单质铁 | B. | 滤渣中一定含有铜,可能含有金属M | ||
| C. | 滤液的质量大于原混合溶液的质量 | D. | 滤液中一定含有两种金属阳离子 |
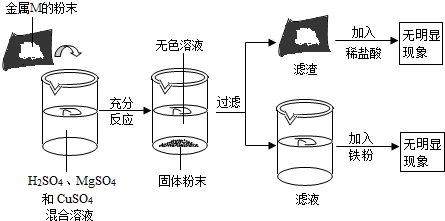
分析 根据题意,将一定质量金属M的粉末加至含有H2SO4、MgSO4和CuSO4的混合溶液中,得到无色溶液和固体粉末,说明了溶液中的铜全部置换出来;过滤后,向滤渣中加入盐酸无明显现象,说明了没有较活泼的金属存在.向滤液中加入铁粉,无明显现象,说明了硫酸完全参加了反应,加入的M金属能与硫酸反应.据此分析判断有关的问题.
解答 解:由题意可知,将一定质量金属M的粉末加至含有H2SO4、MgSO4和CuSO4的混合溶液中,得到无色溶液和固体粉末,说明了溶液中的铜全部置换出来;过滤后,向滤渣中加入盐酸无明显现象,说明了没有较活泼的金属存在.向滤液中加入镁粉,无明显现象,说明了硫酸完全参加了反应,加入的M金属能与硫酸反应,故:
A、由上述分析可知,M能与硫酸、硫酸铜放反应,生成了硫酸亚铁,溶液呈浅绿色,故A结论错误;
B、由上述分析可知,滤渣中一定含有铜,不含有金属M,故B结论错误;
C、由于M不能确定,滤液的质量与原混合溶液的质量的关系无法确定,故C结论错误;
D、由上述分析可知,滤液中一定含有镁和M的阳离子,故D结论正确.
故选D.
点评 解答这类题目时,首先,要熟记和理解金属活动性顺序及其应用,以及与之相关的知识等;然后,根据所给问题情景结合所学的相关知识和技能,细致地阅读、分析题意等细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.


科目:初中化学 来源: 题型:选择题
| A. | 混合气体中一氧化碳质量为1.4g | |
| B. | 碱石灰增重质量为6.6g | |
| C. | 混合气体中碳、氢元素的质量比为9:2 | |
| D. | 混合气体中两种气体分子数之比为3:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验 | 实验现象 | 实验结论 |
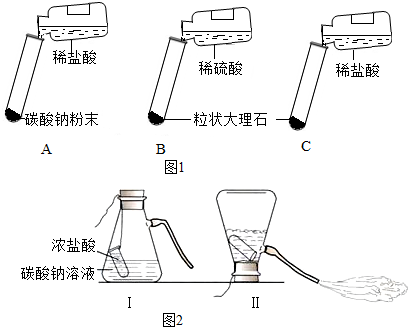
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取二氧化碳 |
| B | 产生气泡,速率迅速减慢,反应几乎停止. | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ①反应较强烈,产生大量气泡 | ②适宜制取二氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
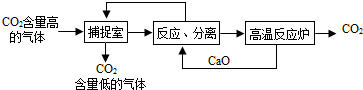
| A. | 该过程可实现CO2零排放 | |
| B. | 整个过程中,有2种物质可以循环利用 | |
| C. | 整个过程中,涉及到两种碱 | |
| D. | “反应并分离”的过程中,分离物质的操作是蒸发、结晶 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用湿润的红色石蕊试纸检验氨气 | |
| B. | 稀释浓硫酸时,将浓硫酸注入盛水的量筒中 | |
| C. | 进行氢气燃烧实验前一定先检验氢气纯度 | |
| D. | 做铁在氧气中燃烧实验时,预先在集气瓶底铺一层细沙 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
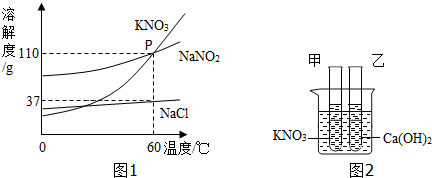
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 等于7 | B. | 小于7 | C. | 大于7 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一瓶浓硫酸溶液的pH=a,将其敞口放置一段时间后溶液的pH=b | |
| B. | 欲用量筒量取amL溶液,俯视刻度线读出读数bmL | |
| C. | 试管内稀盐酸质量为a,加入铜粉一段时间后溶液质量为b | |
| D. | 酒精和水混合前的体积之和为a,混合后总体积为b |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com