
【题目】核电荷数为11~18的元素的原子结构示意图等信息如下,请回答有关问题:
(1)从原子结构角度
①在元素周期表中,以上元素都位于第三周期的原因是_________。
②氩气(化学式为______)的化学性质比较稳定的原因是_________。
(2)写离子符号:①铝离子________,②硫酸根________。
(3)写出氧化镁的化学式并标出元素的化合价:________。
(4)一种氯原子的相对原子质量为37,该氯原子的中子数为________。
【答案】原子的核外电子层数均为3 Ar 原子最外层有8个电子,是一种相对稳定的结构 Al3+ SO42- ![]() 20
20
【解析】
(1)①在元素周期表中,以上元素都位于第三周期的原因是各原子的核外电子层数相同,均为3;②氩气的化学式为Ar,氩气的化学性质比较稳定的原因是氩原子最外层有8个电子,是一种相对稳定的结构;
(2)①铝离子带三个单位的正电荷,可表示为Al3+;②硫酸根可表示为SO42-;
(3)氧化镁中镁元素化合价为+2价,氧元素化合价为-2价,故氧化镁化学式为MgO;其中镁元素为+2价可表示为![]() ;
;
(4)由图可知,氯原子的质子数=原子序数=17,即所有氯原子的质子数均为17,相对原子质量=质子数+中子数,故该氯原子的中子数=相对原子质量-质子数=37-17=20。


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】下图表示某些物质间转化关系。A、C是由相同元素组成的无色液体,且A具有消毒杀菌作用;B、H为黑色固体,F为绿色固体,D、E、G为常见无色气体,E能参加植物的光合作用, X是红色金属。请回答下列问题:
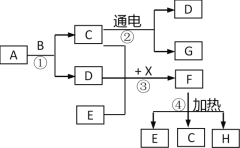
(1)写出C、X的化学式:______,______。
(2)B在反应①中的作用是__________。
(3)写出反应②、④的化学表达式:②_______;④________。
(4)以上①—④的化学反应中,分解反应有_______个(填数字)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)化学用语是学习和研究化学的工具,请用化学用语填空。
①两个汞原子______;
②两个铁离子______;
③氯气______;
④地壳中含量最高的元素和地壳中含量最高的金属元素组成的化合物的化学式______。
(2)请写出![]() 中数字的含义:
中数字的含义:
①“+4”表示______;
②“2”表示______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小雨收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水,其实验过程如图所示。请回答以下问题:
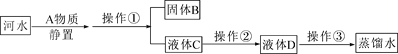
(1)A物质的名称是__________,操作①的名称是__________;
(2)操作②过程主要发生________(选填“物理”或“化学”)变化;
(3)小雨取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是________(选填“软水”或“硬水”)。经过操作③以后,小雨重复上述实验,他观察到的实验现象是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下列微粒模型示意图可能代表水分子的是_______。(选填字母序号)

(2)利用(1)的结论,通过观察NaCl溶解图回答:
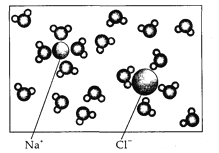
①框内代表的物质是________________;
②请描述框内离子与分子结合时的特点: ____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组对氧气的制取进行了进一步探究。
(1)用高锰酸钾制氧气,对比用向上排空气法和排水法收集到的氧气的纯度。
(进行实验)
①用向上排空气法收集氧气:将带火星的木条放在集气瓶口,当_________时证明氧气集满,用传感器测定集气瓶中氧气的体积分数。重复该实验3次并记录数据。
②用排水法收集氧气:氧气能用排水法收集的原因是____,用传感器测定集气瓶中氧气的体积分数。重复该实验3次并记录数据。
氧气的收集方法 | 向上排空气法 | 排水法 | ||||
氧气的体积分数/% | 79.7 | 79.6 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气的平均体积分数/% | 79.7 | 89.7 | ||||
(实验分析)不考虑操作失误的因素,用排水法也收集不到纯净的氧气,其主要原因是__________。
(2)用过氧化氢溶液制氧气,探究不同催化剂催化过氧化氢分解的效果。
(查阅资料)
①MnO2、Cr2O3、Fe2O3、CuO、S对过氧化氢的分解均具有催化作用。
②海藻酸钠可以作为催化剂的载体支架,形成负载不同催化剂的海藻酸钠微球。
(进行实验)
①制备五种负载不同催化剂(MnO2、Cr2O3、Fe2O3、CuO、S)的海藻酸钠微球,每个微球大小相同,且负载催化剂的质量相等。
②取30粒负载某种催化剂的海藻酸钠微球与20mL质量分数为5%的过氧化氢溶液,在锥形瓶中迅速混合发生反应,实验装置如图1,采集200s内压强数据,绘制曲线如图2。

(实验分析)
①每次实验时,海藻酸钠微球数应相同的原因是_________。
②本实验中,通过一段时间内______来反映生成氧气的快慢。
③本实验中,负载MnO2的微球显示了良好的催化效果,60s时竟将橡皮塞弹飞,在图2中对应的曲线是_______(填“a”或“b”);负载_______的微球催化效果较好,反应温和;负载Fe2O3、Cr2O3的微球催化效果一般;负载_______的微球催化能力最弱。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(5分)下表是元素周期表的一部分,请你根据下表回答问题:
3 Li 锂 6.941 | 4Be[来铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟[来 19.00 | 10 Ne 氖 20.18 |
11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 29.95 |
(1)根据上表回答问题
①钠的相对原子质量是 。
②上表中,金属元素有 种。
(2)图甲是某元素在元素周期表中的部分信息,图乙是该元素的一种粒子结构示意图。
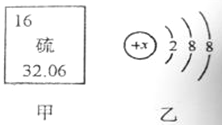
①该元素的原子的核电荷数为 ,该原子的最外层电子数为 。
②图乙所示粒子的符号为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】资料显示,将新制的浓度为5%的过氧化氢溶液加热到80℃时才有较多的氧气产生。而向相同质量的5%的过氧化氢溶液加入二氧化锰,常温下就会立即产生氧气,因此实验室常使用此方法制氧气。
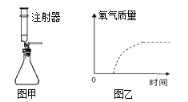
(1)实验室用过氧化氢制氧气的符号表达式为__________________________;
(2)利用图甲作为上述制取氧气的发生装置,注射器相当于___________(填一种仪器名称),它除添加液体试剂外,还具有的作用是__________________。
(3)分别采用两份质量相同且浓度均为5%的过氧化氢溶液制氧气,图乙虚线表示加热分解制取氧气的曲线,请在图中用实线画出加入二氧化锰制取氧气的曲线(假设两种情况下均完全分解)__________________。
(查阅资料)除二氧化锰外,某些物质可以作为过氧化氢溶液分解的催化剂。
(提出猜想)除二氧化锰外,氧化铜也可以作为过氧化氢溶液分解的催化剂。
(完成实验)按下表进行实验,实验数据记录如下:
实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
双氧水的质量和浓度 | 5g、5% | 5g、5% | 5g、5% |
加入的固体及质量 | 无 | MnO2 0.1g | CuO 0.1g |
相同时间内产生氧气的体积 | 3mL | 11mL | 9mL |
(4)本实验中,测量氧气体积的装置应选择________;
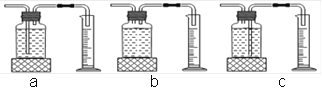
(数据分析)
(5)实验Ⅲ与实验______可知,氧化铜也可以加快过氧化氢分解的速率;
(6)通过比较___________________,发现二氧化锰比氧化铜的催化效果更好。
(讨论反思)
(7)为了最终确定氧化铜是否可以作为过氧化氢分解制氧气的催化剂,大家认为还需要补充完成两个实验:_____________________;___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com