
【题目】下列微粒符号中,对“2”含义的理解正确的是![]()
A.2Cu中的“2”表示2个铜元素
B.![]() 中的“2”表示每个亚铁离子带有2个单位的正电荷
中的“2”表示每个亚铁离子带有2个单位的正电荷
C.![]() 中的“2”表示一个硫化氢分子中含有一个氢分子
中的“2”表示一个硫化氢分子中含有一个氢分子
D.![]() 中化学式上方的“2”表示硫元素为
中化学式上方的“2”表示硫元素为![]() 价
价
科目:初中化学 来源: 题型:
【题目】某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、MgO等。研究小组对其进行综合处理的流程如下:资料①:SiO2、Al2O3可溶于氢氧化钠溶液;资料②:MgCl2溶液加热容易水解产Mg(OH)2。
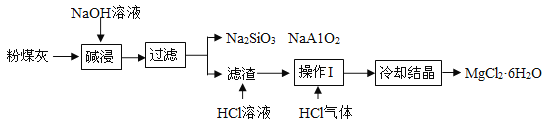
(1)火电厂发电采用的固体燃料主要是煤,化石燃料除煤外还有_____________(填一种即可)。人们开发 和应用的清洁能源有_____________(填一种)。
(2)碱浸溶解SiO2(性质与CO2相似)的反应化学方程式为_____________。
(3)粉煤灰碱浸时通常需要在较高温度下进行,原因是_____________。
(4)滤渣中加入稀盐酸发生反应的化学方程式为___________。
(5)操作I的名称是___________。
(6)加热浓缩时通入HCl气体的目的是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组同学在实验室发现了一瓶标签残缺的无色溶液(常温下,如图所示),为确认其成分,他们进行了如下探究活动。

根据标签受损的情况判断,这瓶试剂不可能是____(填“酸”、“碱” 或“盐”)。
老师提示:无色溶液可能为NaCl溶液、NaOH溶液、Na2CO3溶液和NaHCO3溶液中的一种。
(查阅资料)
四种物质的溶解度信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
(资料分析)
通过对四种物质溶解度信息的分析,这瓶无色溶液一定不是______。
(进行实验)
为了进一步确定无色溶液的成分,化学兴趣小组同学进行了实验,并记录如下。
实验组别 | 实验步骤 | 实验现象 | 实验结论 |
1 | 取无色溶液于试管中,滴加酚酞溶液 | 溶液由无色变为红色 | 无色溶液一定不是_______ |
2 | 取无色溶液于试管中,滴加稀盐酸 | 刚开始无明显现象,一会儿有气泡产生 | 无色溶液是部分变质的NaOH溶液 |
NaOH溶液暴露在空气中容易变质,反应的化学方程式为:_______。
小樊同学对实验2的结论产生了质疑,他通过查阅资料得知:碳酸钠和稀盐酸反应,当稀盐酸的量不足时会生成碳酸氢钠,足量时生成二氧化碳和水。他认为无色溶液也可能是Na2CO3溶液。于是他们又进行了如下探究活动。
实验组别 | 实验步骤 | 实验现象 | 实验结论 |
3 | 取无色溶液于试管中,滴加足量氯化钙溶液,充分反应后过滤,向滤液中滴加氯化镁溶液 | 滴加氯化钙溶液时有白色沉淀生成,过滤后向滤液中滴加氯化镁溶液无明显现象 | 无色溶液是_______ |
(释疑与反思)
碳酸钠和稀盐酸反应,稀盐酸的量不同时生成物也不同。请你再举出一个反应物的量不同时,生成物也不同的例子:________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用适当化学用语填空:
(1)3个亚铁离子_____;
(2)氦气_____;
(3)最简单的有机物_____;
(4)保持氧气的化学性质的微粒_____;
(5)标出纯碱中金属元素的化合价_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明拿起家中的水壶准备煮水时,发现壶内有些褐色的固体。为了探究其成分,与兴趣小组同学查阅资料后获知这些褐色的固体是水垢,它可能是因为水中含有Ca(HCO3)2和Mg(HCO3)2等可溶性物质在加热时生成CaCO3和Mg(OH)2。
(1)含有较多Ca(HCO3)2的水称_____,加热时发生反应的化学方程式为_____。
(2)小明认为该水垢的成分只有CaCO3;但小白不同意,认为也可能只有Mg(OH)2,还可能是_____。
(3)小明为了证明自己的猜想,设计如下实验方案:
实验操作 | 现 象 | 结 论 |
①取少量水垢于试管中,加入过量的_____。 | 观察到现象_____。 | 水垢中有CaCO3 |
②向①反应后的试管中滴加2-3滴NaOH溶液 | 观察到现象_____。 | 水垢中没有Mg(OH)2,我的猜想成立 |
(3)小白不认可小明的结论,认为他的实验操作有缺陷,原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】研究元素知识是学好化学的基础,如表包含部分元素的相关信息,请完成填空。
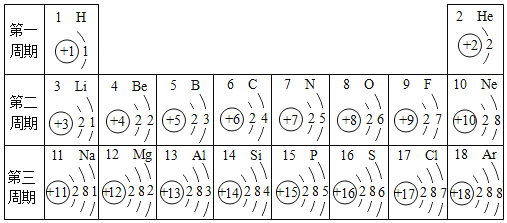
(1)1869年,俄国化学家_____发现了元素周期律并编制了元素周期表;
(2)用正确的化学用语填空:两个氢原子_____;2个氧分子_____;3个亚铁离子_____;氧化铝中铝元素显+3价_____
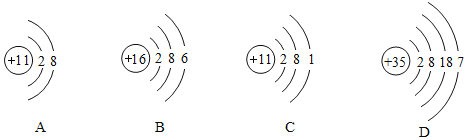
(3)下列图中微粒共表示_____种元素,其中与氯元素具有相似化学性质的是_____![]() 填序号
填序号![]() 。其中D元素位于第_____周期。
。其中D元素位于第_____周期。
(4)写出原子序数为1、6、8、11四种元素所组成化合物的化学式_____。
(5)通过分析,同一横行元素之间的排列有一定的规律,如:①从左到右,由金属元素逐渐向非金属元素过渡;②从左到右,各元素原子的电子层数相同;③_____(任写一条)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列叙述正确的是( )
A. 油脂是重要的营养物质,正常情况下,每人每天需要摄入![]()
B. 废电池中含有铅、镍、镉、汞,若随意丢弃会造成地下水和土壤污染
C. 碘是甲状腺素的重要成分,患有甲状腺肿大的病人应禁止碘的摄入
D. 食品添加剂虽然都是化学合成物质,但可以改善食品品质,可以适量使用
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】NiSO46H2O是一种绿色易溶于水的晶体,广泛用于化学镀镍、生产电池等,可由电镀废渣(除含镍外,还含有Cu、Zn、Fe等杂质)为原料获得。有关工艺流程如图:
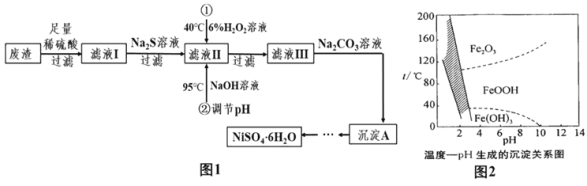
(相关资料)①Ni能与稀硫酸反应生成NiSO4和H2
②ZnSO4+Na2S=ZnS↓+Na2SO4
③H2O2溶液能将FeSO4氧化成Fe2(SO4)3
④NiCO3是一种不溶于水、易溶于强酸的浅绿色沉淀。
(问题解答)
(1)向废渣中加入足量稀硫酸的目的是_____。
(2)在滤液Ⅱ中加入H2O2溶液时,温度不能太高的原因是_____。
(3)除铁时还能加入适量的Na2CO3溶液调节酸度,反应生成Na2SO4、CO2气体和一种浅黄色的黄铁矾钠沉淀[化学式为:Na2Fe6(SO4)4(OH)12],这样可以将Fe3+除去。写出该反应的化学方程式_____。如图是温度—pH与生成的沉淀关系图,图中阴影部分是黄铁矾钠稳定存在的区域。下列说法正确的是_____(填序号)。
A FeOOH中铁元素为+2价
B Fe2O3固体为红色
C 若在25℃时,用H2O2氧化Fe2+,再在pH=4时除去铁,此时溶液中出现的沉淀是FeOOH和Fe(OH)3
D 工业生产中常保持在85~95℃生成黄铁矾钠,此时水体的pH为1.5左右
(4)从“沉淀A”制得NiSO46H2O晶体的实验步骤依次为:向沉淀中加入_____溶液,直至恰好完全溶解,转化为NiSO4溶液;蒸发浓缩、冷却结晶,过滤得NiSO46H2O晶体,用少量乙醇洗涤NiSO46H2O晶体并晾干。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列图示,回答相关问题:
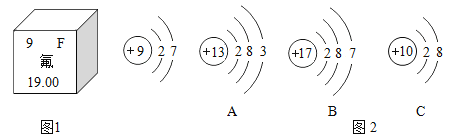
(1) 氟的相对原子质量为___________,氟元素的化学性质与图中______________(填字母序号)化学性质相似。
(2) A在化学变化中容易______________(填“得”或“失”)电子;AB对应的元素组成的物质的化学式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com