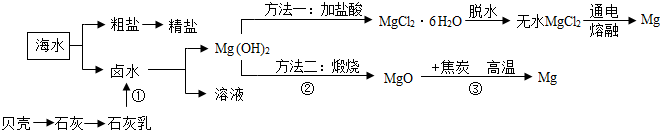
(2005?玄武区一模)2004年6月5日是世界环境日,其主题是“海洋存亡,匹夫有责”,开发海洋,维持海洋的可持续发展是每个地球公民的神圣职责.请回答下面关于海洋的几个问题:
[问题一]去年5月,我国浙江沿海发生大面积的“赤潮”,造成养殖业重大损失.赤潮的发生主要是与因为藻类的疯狂生长,与藻类疯长的密切相关的元素是
N;P
N;P
(填元素符号)
[问题二]海水中资源丰富,含量最多的金属阳离子是
Na+
Na+
(填离子符号),含量最多的分子是
H2O
H2O
(填化学式).
[问题三]我国舟山盐场海水晒盐的原理是
B
B
.(填序号)
A.氯化钠的溶解度受温度影响较大
B.因氯化钠溶解度受温度影响不大,故采取蒸发水分的方法.
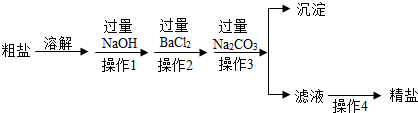
所得粗盐中主要含泥砂、氯化镁、氯化钙等杂质,现对其进行提纯,主要操作流程如下:

(1)操作①的名称是
过滤
过滤
,操作②的名称是
蒸发
蒸发
.
(2)A溶液是
a
a
,B溶液是
d
d
.(选择合适序号填空)
a、Na
2CO
3 b、K
2CO
3 c、H
2SO
4 d、HCl
[问题四]经勘察,深海下含有丰富的“可燃冰”,可满足人类1000年的能源需要.该物质是一种晶体,晶体中平均每46个水分子构建成8个笼,每个笼可容纳1个CH
4分子或1个游离H
2O分子.若晶体中每8个笼只有6个容纳了CH
4分子,另外2个笼被游离H
2O分子填充,则天然气水合物的平均组成可表示为
B
B
.
A、CH
4?14H
2O B、CH
4?8H
2O C、CH
4?(23/3)H
2O D、CH
4?6H
2O
若该水合物可表示为CH
4?nH
2O,则其与氧气完全燃烧的方程式如下,请将括号中的化学计量数补充完整:
CH
4?nH
2O+2O
2CO
2+
n+2
n+2
H
2O.
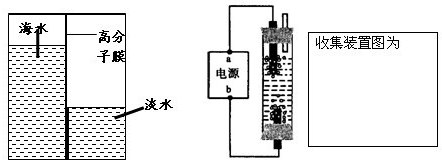
[问题五]海水淡化是国际上研究的热点问题,我国科学家在利用高分子膜进行海水淡化的研究上取得了一些成绩.如图,左侧为海水,右侧为经过一段时间后由左侧经高分子膜渗透得到的淡水,分析高分子膜应具有的性质是
使水分子通过而离子(钠离子、镁离子等)不能通过
使水分子通过而离子(钠离子、镁离子等)不能通过
.
[问题六]如图为刘迪蒙制作的一种家用环保型消毒液发生器:原理是电解饱和氯化钠溶液,制得的消毒液有较强的杀菌能力,该反应是利用氯化钠和水在电解条件下生成NaOH、H
2和Cl
2,请完成化学方程式.
.
该消毒液中起消毒作用的物质是NaClO(次氯酸钠),它是由氯气和NaOH进一步反应制得的,反应方程式为:2NaOH+Cl
2=NaCl+NaClO+H
2O.请模仿写出Cl
2与熟石灰作用制取漂白粉的化学反应方程式:
2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
.
2005年3月29日,在我省淮阴发生氯气(Cl
2)泄漏的重大事故.事故发生后,抢险队员立即疏散当地群众,迅速将正在泄漏的氯气罐推入水中,并用消防车对沉降地面的黄绿色气体(氯气)及水中喷洒碱液,防止氯气对环境的进一步污染和对人员的伤害,以降低氯气对环境的污染.
(1)从以上信息中,你能够分析出氯气化学性质为:
与碱反应,与水反应
与碱反应,与水反应
;
(2)如果实验室制取氯气,你可以用什么方法收集?(画出收集装置图)
(3)假如在离开现场的过程中,你应该采取什么措施保护自己?