
在查阅资料时,小明得知CO2在高温条件下能与木炭反应生成CO。他决定对该反应进行探究。
[提出问题]CO2与木炭在高温条件下反应是否生成CO?
[实验探究]小胡设计了如图27的实验方案,并进行实验。
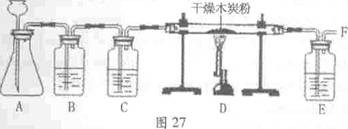
(1)A中用石灰石与稀盐酸反应生成CO2,反应的化学方程式为 。
(2)B中装有饱和碳酸氢钠溶液,其作用是除去CO2气体中混有的少量HCl气体。C中装有浓硫酸。其作用是 。
(3)E中装入氢氧化钠溶液的作用是 。
[实验结论]经检验F处的气体为CO。结论:CO2在高温条件下与木炭反应生成了CO。
[实验反思] (4)有同学对A装置作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端
插入小试管中。改进后的优点是 。
[实验拓展] (5)撤去B,按A→C→D→E顺序连接。然后A中用二氧化锰和过氧化氢溶液混合生成O2,反应的化学方程式为 ① 。此时要检验该实验条件下D中木炭所发生反应的生成物,还需要补充和完善的实验是 ② 。
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:初中化学 来源: 题型:阅读理解
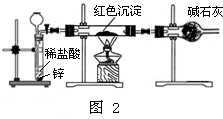 铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.
铜及其化合物是工业生产和日常生活中常用的物质,下面是对铜及其化合物的探究.| 配置用水 | 有浑浊 | 有浑浊 |
| 自来水 | 无浑浊 | 有浑浊 |
| 市售纯净水 | 无浑浊 | 有浑浊 |
| 医用纯净水 | 无浑浊 | 无浑浊 |
| 试验编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 饱和溶液 | 2 | 4 | 6 | 8 | 16 | 32 | 128 |
| 现 象 | 白色浑浊→澄清 | ||||||
查看答案和解析>>
科目:初中化学 来源: 题型:
 20、味精是烹制菜肴时常用的调味品,下面是某品牌味精包装上的部分文字说明.小明觉得上面的信息不能满足对味精的了解,他通过查资料获知关于味精的一些知识.如味精的鲜味与溶液的酸碱度有关,当PH为6-7时鲜味最强;味精的鲜味还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且生成对人体有害的焦谷氨酸钠.据此,他对味精有了正确的认识.
20、味精是烹制菜肴时常用的调味品,下面是某品牌味精包装上的部分文字说明.小明觉得上面的信息不能满足对味精的了解,他通过查资料获知关于味精的一些知识.如味精的鲜味与溶液的酸碱度有关,当PH为6-7时鲜味最强;味精的鲜味还与温度有关,其水溶液经120℃以上长时间加热,不仅鲜味消失,而且生成对人体有害的焦谷氨酸钠.据此,他对味精有了正确的认识.查看答案和解析>>
科目:初中化学 来源: 题型:
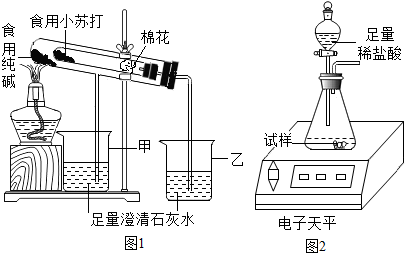
| 名称 | 食用纯碱 | 食用小苏打 |
| 主要成分 | Na2CO3 | NaHCO3 |
| 酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
| 热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
| 称量项目 | 称量时间 | 质量/g |
| 试 样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
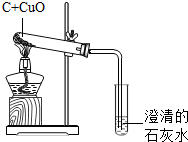 在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如下图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下:
在加热条件下,炭粉可以还原某些金属氧化物,得到金属单质.小明同学设计了如下图所示的实验来研究氧化铜跟活性炭的反应,实验的装置和现象如下: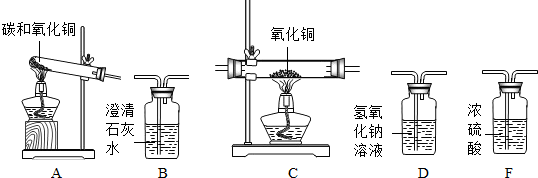
| 实验操作 | 实验现象 | 实验结论 |
| 取7.2g红色固体放入烧杯中,向其中加入足量的稀硫酸,充分反应后,静置 | 若无现象 | 证明红色固体是________ |
| 若______,______ | 证明红色固体中肯定含有 _____,可能含有_____ |
查看答案和解析>>
科目:初中化学 来源:学习周报 化学 沪教课标中考版 2009-2010学年 第16期 总172期 题型:058
小明在化学课上听老师说目前市场上有人从摄影店里低价收购废弃的定影液,以此回收金属银牟取经济利益.联想到姑姑正开着一家影楼.为什么不亲自试试呢?
星期天,小明和伙伴小军一起来到姑姑的影楼,说明了来意.姑姑高兴地说:“看来我的侄子长大了,有经济头脑,行,姑姑答应你.”说完就让店里的小陈阿姨取来了一大瓶废弃的定影液.姑姑说:“你先试试看,如果真行的话,再到姑姑这儿来拿”.“谢谢姑姑”.两人说完就飞快地跑了.
查阅资料:两人回家后,通过Internet网上资料获知:(1)废弃的定影液里含有一定量的AgNO3.(2)铁、铜可从AgNO3溶液中置换出单质银.
设计方案:两人根据化学课上刚刚学过的有关金属的知识,计划分两步进行:(1)加入足够多的铁或铜.(2)除去金属混合物中多余的铁或铜.
交流讨论:
(1)选择加入的金属
小明:可向定影液中加过量的铜粉,充分反应后,过滤.则可得到金属混合物银和铜.
小军:你的方法不可行,我认为应该考虑向定影液中加过量的铁粉,充分反应并过滤,这样就可以得到金属混合物银和铁了,下面的问题就好办了.
聪明的读者,你认为________同学的方案更合理.其原因是________________,该方案涉及到的化学方程式是________.
(2)选择除去银粉中混入的金属的试剂
向过滤后的金属混合物粉末中加入的试剂是________,反应的化学方程式是________.
说到第(2)步时,小明意识到了自己的困难.
进行实验:
(1)小军向废弃的定影液中加过量的铁粉,充分反应后,经过a操作,得到金属混合物.
(2)向金属混合物中加过量的试剂,充分反应后,经过b操作,得到Ag.
请问题:操作a是________,在该操作中用到的玻璃仪器有:________、________和玻璃棒.其中玻璃棒的作用是________.
产品验证:
小明:小军,你如何证明得到的银中就不含过量的铁了呢?
小军:这很简单,周老师不是在课堂上教过我们两种方法吗?
小明:哦,我想起来了,一种是物理方法,还有一种是化学方法.
聪明的读者:您知道这两种方法是:
(1)物理方法:________________.
(2)化学方法:________________.
反思评价:
小军:在这个实验中,根据学过的知识,我们不仅要选择一种金属将AgNO3中的银全部置换出来,还要考虑把多余的这种金属能够很方便地除去.看来我们以后在化学课上还得认真听讲,肯定会学到更多的知识、更好的方法的.
小明(哈哈):对,我们成功了,没想到学习化学不仅有趣,还这么有用.我得赶快把这个妙招告诉姑姑,把这些废弃的定影液都集中起来,既保护了环境,又节约成本,一举两得.何乐而不为呢?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com