
分析 (1)依据质量守恒定律反应前后固体的质量之差即为反应中生成的氧气质量;
(2)利用氧气的质量结合方程式即可求出生成氯化钾的质量和二氧化锰的质量.
解答 解:(1)根据质量守恒定律,生成氧气的质量=14.85 g-10.05 g=4.8 g
(2)设生成氯化钾的质量至少为x,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
149 96
x 4.8 g
$\frac{149}{x}=\frac{96}{4.8g}$
x=7.45 g
二氧化锰的质量为:10.05g-7.45g=2.6g,
答:(1)生成氧气的质量为4.8 g;(2)反应后的剩余固体是氯化钾7.45g,二氧化锰2.6g.
点评 此题是化学方程式的计算考查题,解题的关键是根据质量守恒定律,由反应前后固体物质质量差即反应所产生氧气的质量.


科目:初中化学 来源: 题型:选择题
| A. | NaOH 氢氧化钠 烧碱 | B. | CaO 氢氧化钙 生石灰 | ||
| C. | Na2CO3 碳酸钠 纯碱 | D. | NaCl 氯化钠 食盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
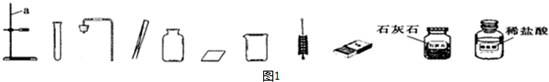
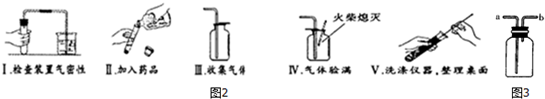
查看答案和解析>>
科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com