
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 一定温度下,某物质的饱和溶液中加入该物质,则溶液溶质质量分数一定增大 | |
| B. | 无色透明的液体一定是溶液 | |
| C. | 升高温度,物质溶解度不一定增大 | |
| D. | 25℃时,100 g物质的饱和溶液中含A25 g,则该物质的溶解度为25 g |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,阅读后计算:
如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,阅读后计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出m克合金样品,将60克稀硫酸分6次慢慢加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出m克合金样品,将60克稀硫酸分6次慢慢加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10克 | n克 |
| 第二次加入10克 | 2.0克 |
| 第三次加入10克 | 1.5克 |
| 第四次加入l0克 | 1.0克 |
| 第五次加入10克 | 0.6克 |
| 第六次加入10克 | 0.6克 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
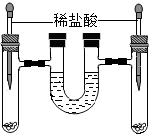 如图,将等质量的锌和铁分别放入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )
如图,将等质量的锌和铁分别放入左、右试管中,加入等质量、等质量分数的稀盐酸,充分反应后,冷却到室温,金属均有剩余,(U型管内为水,初始液面相平,反应过程中装置气密性良好)下列说法正确的是( )| A. | ①③ | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
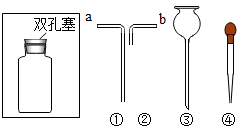
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
|  |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com