
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 矿石样品的质量 | 烧杯和其中混合物的质量 |
| 350g | 12.5g | 358.1g | |
分析 根据反应总质量的变化是因为过程中生成了二氧化碳,所以可求算二氧化碳的质量,进而根据二氧化碳的质量求算碳酸钙的质量,最后求算样品中碳酸钙的质量分数,对比具有开采价值的那个指标进行确定.
解答 解:
(1)根据质量守恒定律可知,生成的二氧化碳的质量为350g+12.5g-358.1g=4.4g
(2)设生成4.4g二氧化碳消耗的碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{44}$=$\frac{x}{4.4g}$
x=10g
则样品中碳酸钙的质量分数为$\frac{10g}{12.5g}$×100%=80%>75%
具有开采价值.
答:(1)反应中生成二氧化碳气体4.4g;
(2)通过计算 该石灰岩矿石中碳酸钙的质量分数为80%,高于开采标志,所以具有开采的价值.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
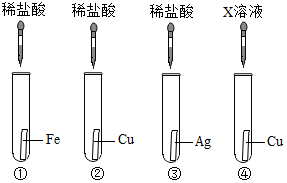 实验课上,化学老师拿来铁、铜、银三种金属,要求同学们设计实验探究它们的活动性顺序.
实验课上,化学老师拿来铁、铜、银三种金属,要求同学们设计实验探究它们的活动性顺序.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 这种氧原子的核外电子数为8 | B. | 这种气体由氧元素组成 | ||
| C. | 这种氧原子的中子数为10 | D. | 这种气体里氧元素的化合价不是零 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
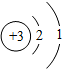 金属锂被誉为“21世纪的能源金属”,当前手机中广泛使用的电池,主要是高能锂电池.请回答下列问题:
金属锂被誉为“21世纪的能源金属”,当前手机中广泛使用的电池,主要是高能锂电池.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 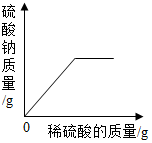 向一定质量的氢氧化钠溶液中加入稀硫酸至过量 向一定质量的氢氧化钠溶液中加入稀硫酸至过量 | |
| B. | 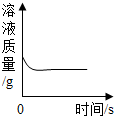 向一定质量的稀硫酸中加入锌片 向一定质量的稀硫酸中加入锌片 | |
| C. | 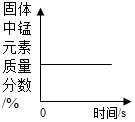 加热一定质量的高锰酸钾固体 加热一定质量的高锰酸钾固体 | |
| D. | 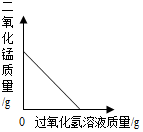 向一定质量的二氧化锰中加入过氧化氢溶液 向一定质量的二氧化锰中加入过氧化氢溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com