
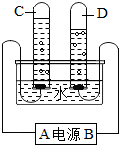
 人类的日常生活和工农业生产都离不开水.请回答下列与水有关的问题:
人类的日常生活和工农业生产都离不开水.请回答下列与水有关的问题:分析 (1)鉴别硬水和软水,最简便的方法是用肥皂水,有大量泡沫的是软水,很少泡沫的是硬水,加热煮沸可以降低水中钙离子、镁离子的含量;
(2)水资源不是取之不尽用之不竭的,我们要节约用水;
(3)有质量守恒定律可知化学反应前后原子的个数和种类不变进行判断;
(4)在电解水实验中,可观察到的现象有:正极的气体体积少,能使带火星的木条复燃,负极的气体体积多,能燃烧,而且体积多的是少的二倍.根据以上现象可推出正极产生的气体是氧气,负极产生的气体是氢气,还能进一步推出水由氢元素和氧元素组成.
解答 解:(1)鉴别硬水和软水,最简便的方法是用肥皂水,有大量泡沫的是软水,很少泡沫的是硬水,加热煮沸可以降低水中钙离子、镁离子的含量,从而降低水的硬度;
(2)农业和园林浇灌植物时,将大水漫灌改为喷灌、滴灌的目的是节约用水;
(3)根据质量守恒定律,反应前后原子种类和个数都不变,由方程式知反应物中含有的原子种类及原子个数为Cl,2;H,2;Na,2;O,2;已知生成物中含有的原子种类及原子个数为Cl,1;H,2;Na,1,O,2;比较分析可知X中含有Na和Cl元素,其原子个数分别为1,故X的化学式为NaCl.
(4)(a)因为电解水时,正极产生氧气,负极产生氢气.产生的氧气和氢气的体积比为1:2.由图可知C、D两试管中的气体体积比为1:2,故可判定C试管中是氧气,所以C管相连的A端为电源的正极;与D相连的B端是负极.
(b)因为电解水时,正极产生氧气,负极产生氢气.化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,由此可以证明水是由氢元素和氧元素组成的;
(c)在水的分解反应中,有新物质氢气和氧气生成,但反应前后参与反应的原子种类没有变化.
故答案为:(1)肥皂水、煮沸;(2)节约用水;(3)NaCl;(4)氧气;负极;2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;氢原子和氧原子.
点评 此题主要考查学生对基础知识和质量守恒定律的实际运用,只有掌握了这一知识的内涵,才能自由驾御,正确解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
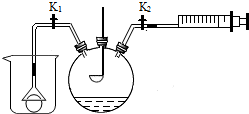 二氧化硫与二氧化碳具有某些相似的化学性质.为研究二氧化硫的性质,化学小组同学用如图所示装置进行实验.关闭K1、K2,将燃烧匙中硫粉在空气中点燃,迅速伸入如图所示瓶中,可以观察到火焰呈蓝紫色,则瓶内的气体是氧气,硫燃烧反应的化学方程式是S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.瓶内的石蕊溶液由紫色变为红色,原因是二氧化硫与水反应生成酸.
二氧化硫与二氧化碳具有某些相似的化学性质.为研究二氧化硫的性质,化学小组同学用如图所示装置进行实验.关闭K1、K2,将燃烧匙中硫粉在空气中点燃,迅速伸入如图所示瓶中,可以观察到火焰呈蓝紫色,则瓶内的气体是氧气,硫燃烧反应的化学方程式是S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2.瓶内的石蕊溶液由紫色变为红色,原因是二氧化硫与水反应生成酸.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 解释或结论 |
| ①取适量的上述无色澄清溶液于试管中,逐滴滴入稀盐酸. | 无明显现象 | 融雪剂中肯定没有[ |
| ②另取适量的上述无色澄清溶液于试管中,滴加几滴碳酸钠溶液. | 产生白色沉淀 | 融雪剂中肯定有 |

查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图所示的照片拍摄于某处天然温泉,请回答下列问题:
如图所示的照片拍摄于某处天然温泉,请回答下列问题:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 溶解度/g | 4.9 | 9.1 | 19.5 | 40.8 | 48.8 | 47.6 | 45.3 | 45 | 43.7 | 42.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com