
 实验小组探究盐酸和氢氧化钠反应过程中溶液 pH 的变化规律,得到如图所示曲线.下列 有关该实验事实的说法正确的是( )
实验小组探究盐酸和氢氧化钠反应过程中溶液 pH 的变化规律,得到如图所示曲线.下列 有关该实验事实的说法正确的是( )| A. | 该实验是将氢氧化钠溶液滴入盐酸中 | |
| B. | B 点表示盐酸和氢氧化钠恰好完全反应 | |
| C. | C 点时的溶液能使酚酞试液变红 | |
| D. | A 点时,溶液中的溶质有氯化钠和氢氧化钠 |
分析 根据氢氧化钠溶液呈碱性,其pH大于7,盐酸呈酸性,其pH小于7,氢氧化钠溶液和盐酸可以发生中和反应,恰好完全反应时其pH等于7,氢氧化钠过量时显碱性,盐酸过量时显酸性进行分析.
解答 解:A、根据图象可以看出,开始时溶液的pH大于7,溶液呈碱性,故是向氢氧化钠溶液中加入稀盐酸,故A错误;
B、B点对应的pH等于7,表明氢氧化钠溶液和稀盐酸恰好完全反应,故B正确;
C、C点的pH小于7,说明酸还没有完全反应,不能是酚酞变红色,故C错误;
D、从图象可以看出,A点的pH大于7,溶液中含有生成的氯化钠和未反应的氢氧化钠,故D正确.
故选:BD.
点评 本题以图象的形式考查了酸碱中和反应过程中溶液pH的变化,完成此题,要抓住曲线变化的趋势和关键点的意义.


科目:初中化学 来源: 题型:选择题
| A. | 冰雪融化 煤气爆炸 | B. | 冰人工降雨 灯泡发光 | ||
| C. | 钢铁生锈 酸雨形成 | D. | 光合作用 酒精挥发 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
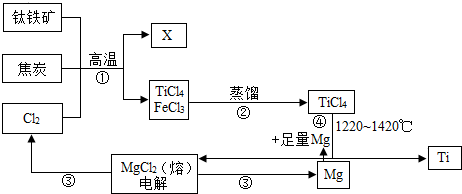
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧化反应一定是化合反应 | |
| B. | 复分解反应中各元素的化合价一定不变 | |
| C. | 置换反应一定有单质生成 | |
| D. | 有盐和水生成的反应不一定是中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
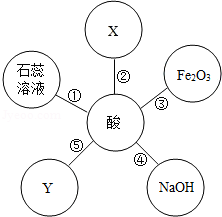 有不同之点.如图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.
有不同之点.如图体现了酸类物质的化学性质,其中X、Y及图中所给其他物质的类别不同.结合此图回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 一定是烧碱溶液 | B. | 一定是酸溶液 | C. | 可能是中性溶液 | D. | 一定是盐溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
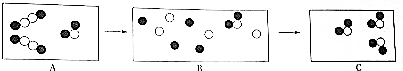
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com