
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
| 溶 解 度/g |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
| KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
| Ca(OH)2 | 0.187 | 0.178 | 0.165 | 0.153 | 0.141 | 0.129 | 0.116 | |


科目:初中化学 来源: 题型:
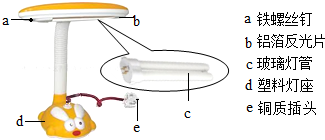 金属材料在生活、生产中的应用非常广泛.
金属材料在生活、生产中的应用非常广泛.查看答案和解析>>
科目:初中化学 来源: 题型:
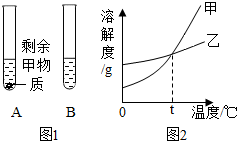 在20℃时,将等质量的甲、乙两种固体,分别加入盛有10g水的A、B
在20℃时,将等质量的甲、乙两种固体,分别加入盛有10g水的A、B查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、若混合物为Fe、Mg,m可能是0.2g |
| B、若混合物为Fe、Zn,m大于0.2g |
| C、若混合物为Fe、Zn,m可能是0.1g,则该混合物中铁的质量分数为50% |
| D、若混合物为Fe、Mg,则稀盐酸中溶质质量分数一定大于7.3% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com