
 如图是某化学反应的微观模型,“○”“
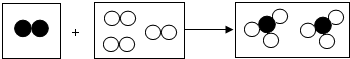
如图是某化学反应的微观模型,“○”“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )| A. | 该反应属于分解反应 | |
| B. | 反应物和生成物中只有一种单质 | |
| C. | 参加反应的两种物质分子个数之比为2:3 | |
| D. | 反应中共有两种元素参与 |
分析 A、根据反应的特点分析反应的类型;
B、根据物质的微观构成,分析物质的类别;
C、根据化学反应的微观模型和质量守恒定律分析参加反应的两种物质分子个数之比;
D、根据原子的种类分析元素的种类.
解答 解:A、由图示可知,该反应的反应物是两种、生成物是一种,该反应是化合反应,故A错误;
B、单质的分子由一种原子构成,化合物的分子由多种原子构成,由图示可知看出反应物是两种单质,而生成物是一种化合物,故B错误;
C、由反应的图示结合质量守恒定律可知,参加反应的两种物质分子个数之比为1:3,故C错误;
D、由反应中原子的种类可知,该反应中共有两种元素,故D正确.
故选:D.
点评 该题关键是从模型图中看出各物质分子的构成,注意解题是要考虑到模型图中每种分子有几个参加反应,利用反应时的微粒个数关系及结构可很轻松的判断.


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:初中化学 来源: 题型:填空题
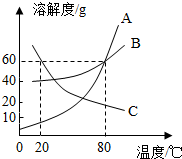 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
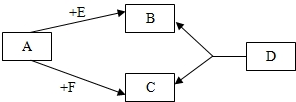 已知A、E、F是单质,B、C、D是化合物,都是初中常见的物质,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.
已知A、E、F是单质,B、C、D是化合物,都是初中常见的物质,它们分别是由碳、氢、氧三种元素中的一种或者几种组成.其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用燃着的木条鉴别氧气和二氧化碳 | B. | 用硝酸银溶液鉴别稀盐酸和食盐水 | ||
| C. | 用水鉴别碳酸钙粉末和碳酸钠粉末 | D. | 用灼烧的方法鉴别棉布和丝绸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 淀粉没有甜味,因此不属于糖类 | B. | 肥皂水可以区别硬水和软水 | ||
| C. | 生铁和钢都是铁的合金 | D. | 钢筋混凝土是复合材料 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验编号 | 选用金属 (均取2g) | 盐酸质量分数 (均取50mL) | 每分钟产生氢气的体积/mL | |||||
| 1分钟 | 1~2分钟 | 2~3 分钟 | 3~4分钟 | 4~5分钟 | 前5分钟共收集气体 | |||
| 1 | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
| 2 | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com