
 因病不能进食者,可以通过点滴葡萄糖、脂肪乳等为人体提供所需能量.
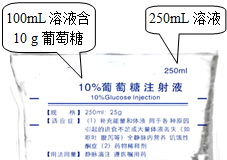
因病不能进食者,可以通过点滴葡萄糖、脂肪乳等为人体提供所需能量.分析 人体的六大营养物质是:水、无机盐、蛋白质、脂肪、糖类和维生素,蛋白质、脂肪、糖类是给人体提供能量的物质.如图是250mL10%的葡萄糖注射液,某同学认为10%是指溶液中葡萄糖的质量分数,这是不正确的,因为本题是指体积分数;1g葡萄糖能提供约4千卡的能量,这袋葡萄糖注射液能为人体提供的能量约是:25克×4千卡每克=100千卡;体重50kg的成人每天需要的能量约2000千卡,若50%的能量由葡萄糖提供,则需要输该规格的葡萄糖注射液的袋数是10;根据化学方程式的计算要准确.
解答 解:(1)如图是250mL10%的葡萄糖注射液,某同学认为10%是指溶液中葡萄糖的质量分数,这是不正确的,因为本题是指体积分数;故答案为:不正确
(2)1g葡萄糖能提供约4千卡的能量,这袋葡萄糖注射液能为人体提供的能量约是:25克×4千卡每克=100千卡;体重50kg的成人每天需要的能量约2000千卡,若50%的能量由葡萄糖提供,则需要输该规格的葡萄糖注射液的袋数是10;故答案为:100 10
(3)根据化学方程式的计算可知,这袋葡萄糖注射液中葡萄糖完全转化为二氧化碳的质量是36.7g,故答案为:36.7;
点评 本考点考查了元素与人体健康的关系和有关计算问题,也是公式的简单应用,基础性比较强,应该好好把握.要合理膳食,均衡营养,保证身体健康.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | 地球上水资源丰富,可随意使用 | |
| B. | 明矾可促使水中悬浮杂质的沉降 | |
| C. | 活性炭能将硬水软化 | |
| D. | 水通电生成氢气和氧气,说明水分子由氢分子和氧分子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 湿衣服晾晒变干是因为分子发生了变化 | |
| B. | 点燃乙醇是因为分子间隔变大了 | |
| C. | 瘪的乒乓球受热鼓起是因为分子变大了 | |
| D. | “酒香不怕巷子深”是因为分子不断运动 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 序号 | 内容 | 实验现象 |
| ① | 常温下将铁丝放在干燥的空气中一个月 | 铁丝表面依然光亮 |
| ② | 常温下将铁丝放在潮湿的空气中一小时 | 铁丝表面依然光亮 |
| ③ | 常温下将铁丝放在潮湿的氧气中一小时 | 铁丝表面略显灰暗 |
| ④ | 常温下将铁丝放在潮湿的空气中一个月 | 铁丝表面已变得灰暗 |
| ⑤ | 将潮湿的铁丝放在高于常温的氧气流中一小时 | 铁丝表面已变得灰暗 |
| A. | 对比①和②说明铁丝生锈需要水份 | |
| B. | 对比②③说明铁丝生锈与氧气浓度有关 | |
| C. | 对比③④说明铁丝生锈需要有氧气 | |
| D. | 对比④⑤说明铁丝生锈的速率与温度有关 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
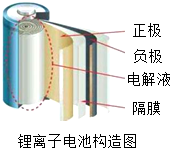 阅读下面科普短文.
阅读下面科普短文.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com