
为了测定某铜锌合金(即铜锌混合物)中锌的质量分数,某同学利用该合金与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下(实验中的误差忽略不计):

(1)试计算该铜锌合金中锌的质量分数.
(2)从上表数据分析,当所取合金与所用稀硫酸的质量比为________时,表明合金中的锌与稀硫酸恰好完全反应.
|
分析:这是一道数据分析题.在分析题目时,关键要抓住几次实验中哪些量不变,哪些量在随什么量的变化而变化,从而分析出在反应过程中哪些数据是完全反应了的,哪些数据没有完全反应. 本题中,由“第一次”与“第二次”实验数据分析,合金质量均为25 g,增加稀硫酸的质量时,产生氢气的质量均为0.4 g,表明此时硫酸过量,而合金中的锌反应完全,因此可用产生氢气的质量0.4 g求出合金中所含锌的质量;从“第三次”实验的数据看,合金质量为50 g时,若硫酸足量,应产生氢气0.8 g,而实验只产生0.4 g氢气,表明此时合金过量,而硫酸反应完全.可见合金质量为25 g,硫酸溶液质量为100 g时,其中锌与硫酸恰好完全反应. |


 优学名师名题系列答案
优学名师名题系列答案科目:初中化学 来源: 题型:
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 10 | 10 | 20 |
| 所用稀硫酸的质量/g | 50 | 80 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验 物质用量 |
第一次 | 第二次 | 第三次 |
| 所取合金的质量/g | 10 | 10 | 10 |
| 所用稀硫酸的质量/g | 50 | 100 | 150 |
| 剩余固体质量/g | 3.5 | 3.0 | 3.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验编号 | 所需合格样品的质量/g | 所取稀盐酸的质量/g | 生成氢气的质量/g |
| 1 | 10.0 | 40.0 | 0.1 |
| 2 | 10.0 | 50.0 | 0.1 |
| 3 | 20.0 | 36.5 | 0.1 |
查看答案和解析>>
科目:初中化学 来源: 题型:
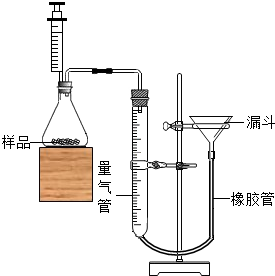 (2013?浦口区一模)Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.
(2013?浦口区一模)Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.| 合金的质量/g | 稀硫酸的体积/mL | 生成氢气的体积/mL | |
| 第一次 | 2 | 15 | 44.4 |
| 第二次 | 2 | 20 | 44.4 |
| 第三次 | 4 | 15 | 44.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量(g) | 10 | 10 | 10 | 10 |
| 充分反应后剩余固体的质量(g) | 8.7 | m | 6.1 | 6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com