


分析 (1)①量取液体时,选择量筒时要遵循:量程应该大于或等于量取的体积;
②称量时,左盘应该放被称量物,右盘应该放砝码;
③配制溶液的操作顺序是:取出药品进行称量,量取液体倒入烧杯中,再进行溶解;
(2)①根据仪器名称解答;
②根据反应物是固体,反应条件是加热,选择给固体加热装置解答;
③根据实验室用块状大理石和稀盐酸反应制取CO2,发生装置应选择固液常温型装置解答;
④进入集气瓶中的水不到五分之一,可从①红磷不足量;②装置的这气密性不好③装置未冷却到室温便打开止水夹来分析.
解答 解:(1)①需要水的质量为:100g-100g×10%=90g,则需要水的体积是90mL,因此应该选择100mL的量筒.
故填:100mL.
②图中操作上的错误是:称量物放右盘,砝码放左盘.
故填:称量物放右盘,砝码放左盘.
③用上述图示的序号表示配制溶液的操作顺序是:取出氢氧化钠,进行称量,再量取水,再把氢氧化钠和水转移到烧杯中,进行溶解.
故填:DACEB.
(2)①仪器a为铁架台;b为酒精灯;答案:铁架台;酒精灯;
②氯酸钾是固体,反应条件是加热,因此发生装置是 B,氯酸钾和二氧化锰混合加热制取氧气,该反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;答案:B;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
③实验室用块状大理石和稀盐酸反应制取CO2,发生装置应选择固液常温型装置,应选用的发生装置是A;由于二氧化碳能溶于水,密度比空大密度大;故采用向上排空气法收集;答案:AC.
④实验完毕,若进入集气瓶中水的体积不到集气瓶中原空气总体积的五分之一,导致这一结果的原因可能是:红磷量不足、装置气密性不好、未冷却到室温就打开止水夹、红磷中含有能燃烧生成其他气体的杂质.故答案为:①红磷量不足;②装置气密性不好;③未冷却到室温就打开止水夹.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:选择题
| A. | X的化学式为H2 | |
| B. | 铜的化合价由0升至+2 | |
| C. | 可采用与制取CO2相同的发生装置制取X | |
| D. | 该反应涉及的物质中,构成粒子有原子、分子、离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 实验步骤及现象 | 结论 | |
| A | ①将少许白色粉末溶于水,得到无色溶液甲 | 白色粉末中一定没有硫酸铜 |
| B | ②在甲中加足量氯化钡溶液,生成白色沉淀乙;过滤得滤液丙 | 白色粉末中可能有碳酸钠、硫酸钠 |
| C | ③在白色沉淀乙中加足量稀硝酸,沉淀部分溶解 | 白色粉末中一定含有硫酸钠和碳酸钠 |
| D | ④在滤液丙中,加入硝酸银溶液,出现白色沉淀 | 白色粉末中一定有氯化钠 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | X、Y、Z都是有机物 | |
| B. | X的化学式是C2H5OH | |
| C. | X中碳、氢元素的质量比为1:3 | |
| D. | 反应前后分子数目、原子数目均不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铝锭难被压缩,因为铝原子间没有间隙 | |
| B. | 若家中燃气泄漏,应立即打开排气扇或抽油烟机 | |
| C. | pH大于5.6的雨水为酸雨,能使紫色石蕊溶液变红 | |
| D. | 生活中为了降低水的硬度往往采用加热煮沸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 是有机化合物 | |
| B. | 柠檬酸中氢元素与氧元素的质量比为8:7 | |
| C. | 碳元素的质量分数为37.5% | |
| D. | 一个柠檬酸分子由6个碳原子、8个氢原子和7个氧原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
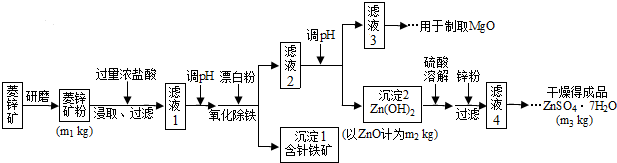
| Mg(OH)2 | Zn(OH)2 | |
| 开始沉淀的pH | 10.4 | 6.4 |
| 沉淀完全的pH | 12.4 | 8.0 |
| 开始溶解的pH | -- | 10.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com