
| A. | 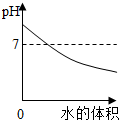 向pH=9的NaOH溶液中不断加水 | B. | 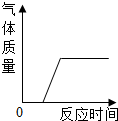 在久置的NaOH溶液中加入盐酸 | ||
| C. | 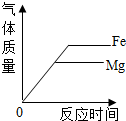 分别向稀盐酸中加入等质量Fe和Mg | D. | 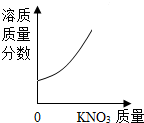 在饱和KON3溶液中加入KNO3晶体 |
分析 根据具体物质的性质进行分析,碱溶液加水稀释碱性减弱;久置的氢氧化钠中含有碳酸钠;镁的活动性比铁强,产生氢气的速率比铁块;一种物质的饱和溶液中再加入该物质不再溶解.
解答 解:A、碱溶液加水稀释碱性减弱,其PH将会减小,但不会小于7,故A错误;
B、久置的氢氧化钠中含有碳酸钠,在久置的氢氧化钠中加入盐酸,就是氢氧化钠和碳酸钠与盐酸的反应,酸碱反应后在于碳酸钠反应,故B正确;
C、镁的活动性比铁强,产生氢气的速率比铁块,不会出现速率相同的情况,故C错误;
D、在饱和硝酸钾溶液中加入硝酸钾不再溶解,故其溶质质量分数不变,故D错误,
故选B.
点评 通过回答本题知道了图象的画法和分析问题解决实际问题的能力.


 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案科目:初中化学 来源: 题型:解答题
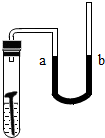 金属是一种非常重要的资源,在生产、生活中有着广泛的用途.
金属是一种非常重要的资源,在生产、生活中有着广泛的用途.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH溶液(Na2CO3) | 加入适量的Ca(OH)2溶液、过滤 |
| B | CO(CO2) | 通过足量的NaOH溶液、干燥 |
| C | CaO(CaCO3) | 加水溶解、过滤 |
| D | FeSO4溶液(H2SO4) | 加入足量Fe粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只有① | B. | 全部错误 | C. | 只有②③④ | D. | 只有①②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
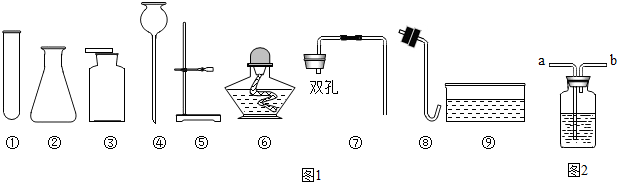
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ③④⑥ | B. | ②③⑤ | C. | ①③⑥ | D. | ④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com