
分析 (1)根据16%的氯化钠溶液与水的密度,进行分析解答.
(2)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(3)实验室配制100g5%的NaCl溶液操作步骤分别是:计算、称量、溶解,根据各操作确定所需要使用的仪器.
(4)溶质质量分数变大,则可能是溶质质量偏大或溶剂质量偏小,可以分析出可能造成这两个方面错误的原因,进行分析解答即可.
解答 解:(1)16%的氯化钠溶液可以使瘪种子浮起,成熟种子下沉,而水密度较它小,起不到选择作用.
(2)溶质质量=溶液质量×溶质的质量分数,配制80g16%的氯化钠溶液,需氯化钠的质量=80g×16%=12.8g;溶剂质量=溶液质量-溶质质量,则所需水的质量=80g-12.8g=67.2g;水的密度为1g/cm3,则根据V=mρ=495.5g1g/cm3=495.5mL.
(3)配制80g16%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解;在这些操作中需要的仪器:托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒.
(4)用量筒量取水时,俯视液面,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大(合理即可).
故答案为:(1)该浓度的溶液可以使瘪种子浮起,成熟种子下沉,而水密度较它小,起不到选择作用;
(2)12.8;67.2;
(3)①③⑤⑥⑩;
(4)量筒量取水时,俯视液面(合理即可).
点评 本题难度不大,掌握配制溶质质量分数一定的溶液的基本步骤,明确导致溶质质量分数变大的因素等是正确解答本题的关键.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
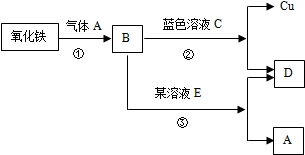
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
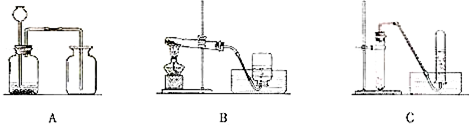
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
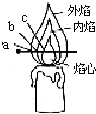 化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.
化学兴趣小组的三位同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用观察颜色的方法区别氮气和二氧化硫 | |
| B. | 用过滤的方法除去水中混有的氯化钠 | |
| C. | 用闻气味的方法区别氧气和二氧化碳 | |
| D. | 用蒸发的方法区别海水和蒸馏水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com