
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-。现取两份200mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体0.68g;②第二份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
A.一定不存在Ba2+,NH4+可能存在B.CO32-一定存在
C.Na+一定不存在D.一定不存在Cl-
【答案】B
【解析】
根据①可知生成的气体为氨气,其质量为0.68g,可求出溶液中铵根离子的质量为:![]() ;根据②可知2.33g沉淀为硫酸钡,6.27g沉淀为硫酸钡和碳酸钡的混合物,碳酸钡的质量为:6.27g-2.33g=3.94g;则原溶液中一定存在CO32-、SO42-;根据离子共存,溶液中一定不存在Ba2+;同时可以求出溶液中硫酸根的质量为:
;根据②可知2.33g沉淀为硫酸钡,6.27g沉淀为硫酸钡和碳酸钡的混合物,碳酸钡的质量为:6.27g-2.33g=3.94g;则原溶液中一定存在CO32-、SO42-;根据离子共存,溶液中一定不存在Ba2+;同时可以求出溶液中硫酸根的质量为:![]() ;溶液中碳酸根的质量为:
;溶液中碳酸根的质量为:![]() ;由于个数比等于质量除以相对分子质量之比,溶液中铵根:硫酸根:碳酸根的个数比=
;由于个数比等于质量除以相对分子质量之比,溶液中铵根:硫酸根:碳酸根的个数比=![]() ;根据化学式可知,一个碳酸根与两个铵根结合成碳酸铵,一个硫酸根与两个铵根结合成硫酸铵;若无其他离子,溶液中的阳离子与阴离子电荷数之比为:
;根据化学式可知,一个碳酸根与两个铵根结合成碳酸铵,一个硫酸根与两个铵根结合成硫酸铵;若无其他离子,溶液中的阳离子与阴离子电荷数之比为:![]() ; 根据溶液中阴阳离子的电荷数守恒得,可得阳离子数目不够,需要另外的阳离子,因此溶液中还肯定有Na+;由于没有对氯离子的存在进行检验,因此不能确定溶液中是否含有氯离子,根据分析可知,原溶液中一定存在Na+、NH4+、CO32-、SO42-;一定不存在Ba2+,可能含有Cl-。
; 根据溶液中阴阳离子的电荷数守恒得,可得阳离子数目不够,需要另外的阳离子,因此溶液中还肯定有Na+;由于没有对氯离子的存在进行检验,因此不能确定溶液中是否含有氯离子,根据分析可知,原溶液中一定存在Na+、NH4+、CO32-、SO42-;一定不存在Ba2+,可能含有Cl-。
故选B


科目:初中化学 来源: 题型:
【题目】水是生产、生活及实验室中经常用到的物质。

(1)人们常用_____鉴别软、硬水。
(2)配制一瓶符合如图1所示规格的氯化钠溶液,某同学量取水时,如果按照图2的方法读数,则所配制的溶液中溶质质量分数会_____(填“偏大”或“偏小”或“不变”)。
(3)若用15%的氯化钠溶液来配制如图1所示规格的氯化钠溶液,需要加水的质量为_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下表示的是碳及其化合物的相互转化关系
![]()
其中涉及的基本反应类型依次为( )
A.置换、化合、分解、复分解B.置换、化合、复分解、分解
C.化合、置换、分解、复分解D.化合、置换、复分解、分解
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】黄铜矿经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4,利用以下实验可制取补血剂原料碳酸亚铁并回收铜。
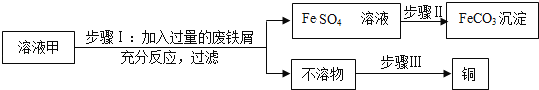
步骤I中,发生反应的化学方程式包括:
①Fe2(SO4)3+Fe→3FeSO4,
②_____,
③_____。
步骤II中加入一种试剂(Na2CO3)可实现其转化,将试剂(Na2CO3)进行焰色反应,观察得到的火焰颜色是__________色。
步骤III回收铜的主要实验操作包括:①过滤,②加足量稀硫酸,③洗涤、干燥,正确的操作顺序是_____(填序号)。
若废铁屑含有少量铁锈,对回收铜_____(填“有”或“无”)影响。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】稀盐酸与氢氧化钠溶液混合后,发现溶液仍为无色。为了证明她们确实发生了化学反应,某学习小组进行如下实验:
|
|
图1 | 图2 |
| |
图3 | |
① 图1中从a→b整个实验过程中观察到的现象是_________________,由此证明上述实验过程确实发生了化学反应。
② 图2表示反应过程中溶液的PH变化情况,c点表示的意义是________________;当溶液的pH=2时,此溶液的溶质有_______________。
③ 图3表示向一定量的氢氧化钠溶液中逐滴加入稀盐酸至过量,图像中能正确反应对应变化关系的是________________。
④ 为测定氢氧化钠溶液的质量分数,取氢氧化钠溶液50g,用10%的稀盐酸进行测定,当加入稀盐酸为36.5g时恰好完全反应。
I. 稀盐酸中含HCl的物质的量是_____mol;
II. 氢氧化钠溶液的质量分数是___________。(根据化学方程式列式计算)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】70 ℃时,将100 g溶质的质量分数为20%的R溶液不断降温,析出固体R的质量与温度的变化关系如下图所示。根据图像回答下列问题:
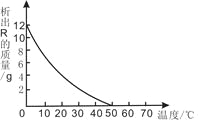
(1) R的溶解度随温度的升高而______________(填“增大”、“不变”或“减小”);
(2)从70 ℃降到50 ℃的过程中,该溶液中溶质的质量分数_________(填“变大”、“变小”或“不变”);
(3)要配制50℃时50 g R的饱和溶液,需要R的质量是 ________ g , 需要的玻璃仪器有_________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在实验室开放日,请用如图所示仪器或装置进行实验。
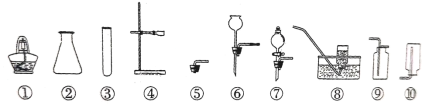
(1)使用仪器①的注意事项是________________。(一条即可)
(2)军军用②⑤⑧组装制取氧气的实验装置,他选择的实验药品为_________________。
(3)实验室可将③④⑦与___________(填标号)连接制取并收集二氧化碳;该发生装置与③④⑥组装成的发生装置相比较,突出优是____________________________。
(4)实验室可以用加热氯化铵和熟石灰固体混合物的方法制取氨气。氨气是一种密度比空气的小,极易溶于水的气体。你制取并收集氨气的实验装置组合是③④_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室提供以下常用仪器,供完成氧气制取时选用(不可重复选用).
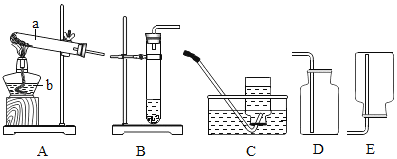
(1)写出有编号仪器的名称:a_____b_____
(2)若选用B装置来制取氧气,反应的化学方程式为:_____若需收集一瓶干燥的氧气,收集装置可选用_____(选填图中编号〕;
(3)如果集气瓶中收集了0.64g氧气,计算该氧气的物质的量是多少?_____若用足量的铁丝在瓶中燃烧,理论上至少需要多少物质的量的铁丝?(通过化学方程式列式计算)_____
(4)某兴趣小组想研究氮气的性质,有同学提出利用空气为原料,通过下列装置除去空气中的氧气.B中的是氢氧化钠溶液,作用是吸收二氧化碳气体.甲物质若是碳粉,写出A中发生的化学方程式_____;当C中见到_____现象时表示气体收集满了.
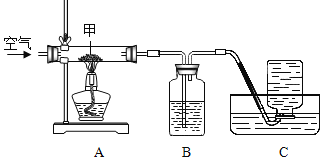
(5)C中收集到的氮气往往不纯,除了水蒸气外,还有少量的稀有气体.还有同学提出,收集到的气体中还可能有少量的氧气,理由是_____(只要填写一种即可).若要使实验装置简单,去掉装置“B”则甲物质可以改用_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对石灰石样品进行如下实验取12g样品放入烧杯中,将100g稀盐酸分4次加入到烧杯中,充分反应后(杂质不溶于水,也不与酸反应),测得剩余固体的质量记录如下。请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
剩余固体的质量/g | 8 | 4 | 2 | 2 |
求:
(1)样品中碳酸钙的质量为_____g:
(2)第4次加入稀盐酸后所得溶液中CaCl2的质量分数_______。(写出计算过程,最终结果保留0.1%)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com