
【题目】实验是化学重要的组成部分
实验内容 | 实验现象 | 实验分析 |
实验一: 将一小根生锈的铁丝放入一定量稀盐酸里 | 若盐酸是足量,可观察到的完整现象是:铁锈逐渐溶解,______ | 请写出盐酸与铁锈主要成分反应的化学方程式______ |
待铁丝全部溶解,向溶液中滴加硝酸银溶液,可观察到白色沉淀 | 该沉淀的化学式是________ 有同学认为这现象不足以证明反应后盐酸有剩余,理由是________ | |
实验二: 在 | 如果滤渣呈银白色 | 滤液中的溶质一定含有________ |
如果滤液呈蓝色 | 滤渣中的滴加足量盐酸,能否观察到气泡?______ | |
如果用铜棒代替锌粉,可观察到的现象是______ | 请写出反应的化学方程式______, 该反应的基本类型是______ |
【答案】溶液变黄,过一段时间,铁丝包面产生气泡,溶液变成浅绿色 Fe2O3+6HCl=2FeCl3+3H2O AgCl 铁丝完全反应后生成的氯化亚铁也能与硝酸银反应生成氯化银沉淀 硝酸铜和硝酸锌 否 铜棒上形成银白色固体,溶液逐渐变蓝 Cu+2AgNO3=Cu(NO3)2+2Ag 置换反应
【解析】
将一小根生锈的铁丝放入足量稀盐酸里,观察到的现象是铁锈逐渐溶解,溶液变黄,过一段时间,铁丝包面产生气泡,溶液变成浅绿色,故填溶液变黄,过一段时间,铁丝包面产生气泡,溶液变成浅绿色;
铁锈的主要成分是氧化铁,氧化铁与盐酸反应生成氯化铁和水,故反应的化学方程式写为:Fe2O3+6HCl=2FeCl3+3H2O;
硝酸银与溶液中的氯离子反应生成氯化银沉淀,其化学式为AgCl,故填AgCl;
铁丝完全反应后生成的氯化亚铁也能与硝酸银反应生成氯化银沉淀,无法证明反应后盐酸有剩余,故填铁丝完全反应后生成的氯化亚铁也能与硝酸银反应生成氯化银沉淀;
滤渣呈银白色,说明硝酸铜没有参加反应,锌与硝酸银反应生成硝酸锌和银,所以滤液中的溶质一定含有硝酸铜和硝酸锌,故填硝酸铜和硝酸锌;
滤液呈蓝色,说明硝酸铜有剩余,则加入的锌粉完全反应,滤渣中不含锌,向滤渣中的滴加足量盐酸,不会生成氢气,也就不能观察到气泡,故填否;
铜棒与硝酸银反应生成硝酸铜和银,在铜棒上形成银白色固体,溶液逐渐变蓝,故填铜棒上形成银白色固体,溶液逐渐变蓝;
铜与硝酸银反应生成硝酸铜和银,故反应的化学方程式写为:Cu+2AgNO3=Cu(NO3)2+2Ag;
由化学方程式可知,该反应是一种单质与一种化合物反应生产另一种单质与化合物的反应,属于置换反应,故填置换反应。


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:初中化学 来源: 题型:
【题目】木炭作为还原剂用于金属冶炼已有几千年历史。教材用如图Ⅰ实验介绍这一知识。
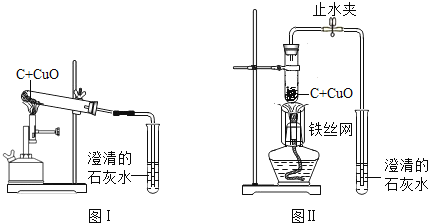
(1).木炭与氧化铜反应的化学方程式是______。
(2).酒精灯火焰处加有铁丝网罩,其作用是______。
(3).固定试管时,试管口要略向下倾斜,其目的是______。
(4).图Ⅰ与教材中的装置还是略作了改进,实验结束时,可先用弹簧夹夹紧橡皮管,再熄灭酒精灯,这样做的目的除了防止石灰水倒吸入热的试管,使试管炸裂外,还可以防止______。
(5).为了提高成功率,某研究小组设计如图Ⅱ方案进行实验。
(实验研究)
分别称取2g木炭与![]() 混合物,按每种比例重复实验3次。实验记录如下表:
混合物,按每种比例重复实验3次。实验记录如下表:
总质量相同(2g)但木炭与![]() 比例不同的实验对比表
比例不同的实验对比表
比例 | 1:6 | 1:7 | 1:8 | 1:9 | 1:10~1:11 | 1:12 | 1:13 |
加热时间 |
|
|
|
|
|
|
|
实验现象 | 红热,产生大量气泡,石灰水变浑浊 | 偶尔红热,气泡较少 | |||||
实验结果 | 表层铜球较大,出现未完全反应的黑色木炭粉末,且木炭含量越高黑色粉末越多 | 反应较完全,生成亮红色网状铜块 | 部分生成 | 主要产物是 | |||
由实验数据分析,除温度外,影响实验的因素是______;
从产物分析,该反应混合物的最佳比例范围是______。
(装置改进)
稳定的高温是本实验成功的关键因素之一,实验装置也会影响加热的效率。图Ⅱ装置将卧式装置改为直立式装置。实验时,将反应混合物夯实于试管底部,调节酒精灯使外焰完全包围试管的下部。你认为该设计是否更好?______(填“是”或“否”);理由是______。
(交流讨论)
由于试管中有空气,实验时应注意:
①混合物需进行预热,除了使试管受热均匀外,另外的目的是______。
②从理论上讲,并不能把石灰水变浑浊作为木炭跟![]() 开始反应的充分证据。其理由是______。
开始反应的充分证据。其理由是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某课外活动小组在学习了书本“空气中氧气含量测定”试验后,对该实验进行了改进。
(实验回顾)图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置。
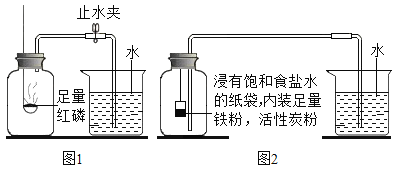
(1)写出红磷燃烧的符号表达式____________________________.
(2)写出该实验的现象__________________。
(问题提出)有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大。
(实验改进)
Ⅰ。根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气含量。装置中饱和食盐水、活性炭会加速铁生锈,通过铁生锈来消耗瓶中的氧气。
Ⅱ。测得实验数据如表
测量项目 | 实验前 | 实验后 | |
烧杯中水的体积 | 集气瓶(扣除内容物)和导管的容积 | 烧杯中剩余水的体积 | |
体积/mL | 80.0 | 126.0 | 54.5 |
(交流表达)
根据表中数据计算,改进实验后测得的空气中氧气的体积分数是___________(计算结果精确到0.1%).
改进后的实验优点是:_______________(写一条)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有四只烧杯,分别盛有稀盐酸、饱和石灰水、碳酸钠溶液中的一种,现向其中滴加了酚酞或石蕊溶液(如图所示).
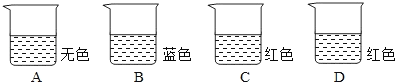
已知:碳酸钠溶液呈碱性,氯化钙溶液呈中性.兴趣小组同学向D中加入足量氯化钙溶液,溶液变浑浊,红色消失变为无色;A和C烧杯液体混合,没有气泡产生也没有沉淀生成,但是混合溶液为无色。以下是相关判断:
①A烧杯中滴加的液体指示剂为酚酞溶液
②向B中加入足量稀盐酸,一定会形成无色溶液
③D原来盛装的是碳酸钠溶液
④C和D混合,会产生白色浑浊,溶液一定仍为红色。
⑤A和C烧杯液体混合后溶液中除指示剂外溶质只有一种
⑥C中加入生石灰,溶液会变浑浊;
下列正确的是( )
A.①②③⑥B.①③④⑥C.①④⑤⑥D.①③⑤⑥
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为从废铜屑中得到较纯的单质铜设计了如下方案。有关说法正确的是 ( )
![]()
A.若X是铁,第③步反应还会生成氯化铁
B.X还可以是Zn,但不能是Ag
C.不需要第②步操作,直接进行第③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是同学们构建的关于氧气的部分知识网络,请你由图回答:
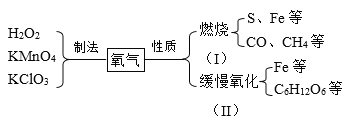
(1)实验室制取氧气的一个化学方程式_____。
(2)硫在氧气中燃烧的现象是_____。I、II两类有氧气参加的化学反应的相同点是(写一条)_____。
(3)从正反两方面举例说明氧气与人类生活的关系_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图表示汽车尾气净化器处理尾气的过程,其主要反应原理为:2NO+2CO![]() 2CO2+N2,下列有关叙述错误的是( )
2CO2+N2,下列有关叙述错误的是( )
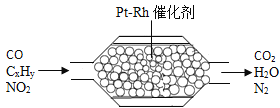
A.CO氧化为CO2所需的氧来源于NO
B.该反应是置换反应
C.Pt﹣Rh催化加在化学反应前后质量不变
D.使用该净化器能减少酸雨的发生
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学常用的实验装置,请回答下列问题。
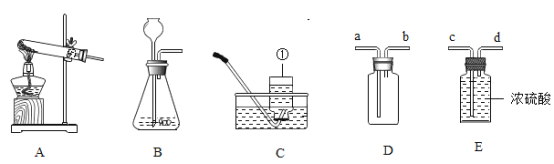
(1)仪器①的名称____________。
(2)实验室制取O2、CO2、H2均可选择________(填装置代号)作为气体的发生装置。
(3)实验室不使用催化剂就能制取O2的化学方程式为_______________,属于_________反应(填“化合”“分解”“置换”或“复分解”)。
(4)实验室制取二氧化碳的化学方程式为____________________,若要收集干燥的二氧化碳气体需要将E装置中________端与D装置中________端相连接(填导管字母代号)。
(5)某气体可用C装置来收集,因为该气体_____________。
(6)组装A装置时,应遵循______________(“从上到下”或“从下到上”)的顺序操作。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如图所示,请回答问题:
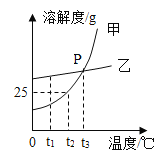
(1)t1℃时,甲、乙两种物质的溶解度大小关系为甲_____乙(填“<”“>“或“=”);
(2)P点的含义_____;
(3)t2℃时,把20g固体甲放入50g水中,充分搅拌,所得溶液的质量是_____g;
(4)欲将t2℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是_____;
(5)如果甲物质中含有少量乙物质,若要提纯甲,一般采用_____的方法。
(6)若将t3℃时甲和乙的饱和溶解降温至t1℃时,所得溶液的溶质质量分数关系为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com