
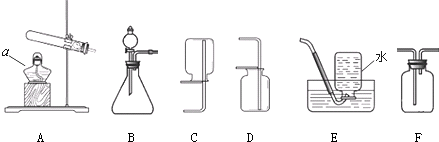
 K2MnO4+MnO2+O2↑;检查装置气密性的方法是连接仪器,将导气管一端放入水中,用手紧握试管,若导管口有气泡产生,则装置气密性良好,反之,则不好;氧气可以用排水法收集,其原因是原因是氧气不易溶于水且不与水反应;又氧气的密度比空气大,还可用向上排空气法收集,因此还可以用于收集氧气的装置是DF;
K2MnO4+MnO2+O2↑;检查装置气密性的方法是连接仪器,将导气管一端放入水中,用手紧握试管,若导管口有气泡产生,则装置气密性良好,反之,则不好;氧气可以用排水法收集,其原因是原因是氧气不易溶于水且不与水反应;又氧气的密度比空气大,还可用向上排空气法收集,因此还可以用于收集氧气的装置是DF;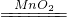 2H2O+O2↑;
2H2O+O2↑; K2MnO4+MnO2+O2↑;连接仪器,将导气管一端放入水中,用手紧握试管,若导管口有气泡产生,则装置气密性良好,反之,则不好;氧气不易溶于水且不与水反应;D、F;
K2MnO4+MnO2+O2↑;连接仪器,将导气管一端放入水中,用手紧握试管,若导管口有气泡产生,则装置气密性良好,反之,则不好;氧气不易溶于水且不与水反应;D、F;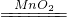 2H2O+O2↑;固体与液体混合常温制气体;
2H2O+O2↑;固体与液体混合常温制气体;

 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

| 加热 |
| 加热 |
| 二氧化锰 |
| 二氧化锰 |
| 点燃 |
| 点燃 |
查看答案和解析>>
科目:初中化学 来源: 题型:
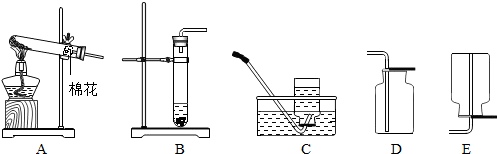
查看答案和解析>>
科目:初中化学 来源: 题型:
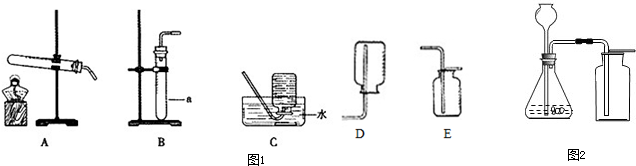
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com