
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁. | 试管外壁发热 | 原因是氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐滴加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体. | 样品中含有的杂质是碳酸钠 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂质是氯化钠 |
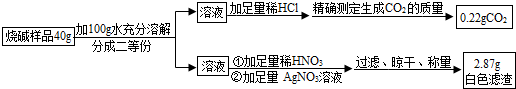
分析 二氧化碳与氢氧化钠反应生成碳酸钠和水,因此可能有碳酸钠;氯化钠可能没有全部反应,因此可能有氯化钠.加水溶解,试管外壁发热,原因是氢氧化钠固体溶于水放热;向①所得的溶液中逐渐加入稀硝酸至过量,一开始无明显现象,一段时间后产生能使澄清石灰水浑浊的气体,因此样品中含有的杂质是碳酸钠;向②所得的溶液中滴加几滴硝酸银溶液,产生白色沉淀氯化银,说明样品中还含有的杂质是氯化钠;
解答 解:(1)二氧化碳与氢氧化钠反应生成碳酸钠和水,因此可能有碳酸钠;氯化钠可能没有全部反应,因此可能有氯化钠;故答案为:CO2+2NaOH=Na2CO3+H2O;可能有少量的氯化钠没有反应;
(2)加水溶解,试管外壁发热,原因是氢氧化钠固体溶于水放热;向①所得的溶液中逐渐加入稀硝酸至过量,一开始无明显现象,一段时间后产生能使澄清石灰水浑浊的气体,因此样品中含有的杂质是碳酸钠;向②所得的溶液中滴加几滴硝酸银溶液,产生白色沉淀氯化银,说明样品中还含有的杂质是氯化钠;上述实验中稀硝酸不可以用稀盐酸代替,因为盐酸中有氯离子,影响氯化钠中氯离子的检验.故答案为:氢氧化钠固体溶于水放热;碳酸钠;氯化钠;不正确;
(3)设20g样品中含有碳酸钠的质量为x,氯化钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 0.22g
$\frac{106}{x}=\frac{44}{0.22g}$
x=0.53g
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
y 2.87g
$\frac{58.5}{y}=\frac{143.5}{2.87g}$,
y=1.17g
氢氧化钠的质量分数=$\frac{20g-(0.53g+1.17g)}{20g}$×100%=91.5%,
答:氢氧化钠的质量分数是91.5%
故答案为:91.5%.
点评 本考点属于实验探究题,既有物质性质的检验,又有化学方程式的书写和有关的计算,综合性比较强.本题根据题目提供的信息,结合实验探究的一般步骤和碱的性质等知识来解决,还要注意化学方程式的书写和配平,有关的计算要准确.本考点主要出现在实验题中.


 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 剩余物质的质量/g | 13.5 | 13.0 | 12.5 | 12.1 | 11.9 | 11.9 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是一种最常见的溶剂,自然界中的水都不是纯净物 | |
| B. | 酸雨的形成与大气中SO2等酸性污染物增多有关 | |
| C. | 水中N、P元素的增多会引起水体的富营养化污染,引起赤潮和水华 | |
| D. | pH=0的水溶液,是中性的溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铁丝在氧气中燃烧生成黑色固体:4Fe+3O2 $\frac{\underline{\;点燃\;}}{\;}$ 2Fe2O3 | |
| B. | 医疗上用氢氧化镁中和过多胃酸:Mg(OH)2+H2SO4═MgSO4+2H2O | |
| C. | 正常雨水的pH约为5.6的原因:CO2+H2O═H2CO3 | |
| D. | 证明铁是金属活动顺序表中氢之前的金属:2Fe+6HCl═2FeCl3+3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com