
| 序号 | 实验步骤 | 实验现象 | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水 | 固体溶解 | 过碳酸钠易溶于水, 能与水发生反应. |
| ② | 向序号①的所得溶液中加入适量的二氧化锰粉末 | 有大量气泡 产生 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 序号②试管中产生的气体是; 过碳酸钠溶于水能生成过氧化氢. |
| ④ | 取序号③试管中的上层清液加入氯化钙溶液 | 产生白色 沉淀 | 反应的化学方程式Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| 小结 | 过碳酸钠与水反应的化学方程式是Na2CO4+H2O═Na2CO3+H2O2. | ||
分析 【实验探究一】①过碳酸钠溶于水时,反应生成碳酸钠和过氧化氢;
③过氧化氢遇二氧化锰能分解生成氧气,所以可以用带火星的木条来检验;
④碳酸钠能和氯化钙反应生成碳酸钙沉淀,根据反应物、生成物和条件书写方程式;
实验小结:根据质量守恒定律和过碳酸钠与水反应的规律书写化学方程式.
【实验探究二】
(1)根据氢氧化钠可以与二氧化碳反应,除去二氧化碳分析;
(2)根据实验要求分析解答;
(3)根据碱石灰的成分和作用分析;
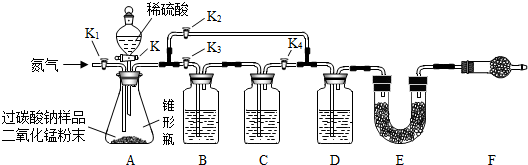
(4)根据碳酸钠与硫酸反应生成硫酸钠、水和二氧化碳;当气体通过浓硫酸时被干燥,通入E中装入碱石灰吸收其中的二氧化碳,利用二氧化碳的质量求出样品中过碳酸钠的含量;
(5)E、F均装入干燥的碱石灰,F装置可以防止空气中的成分进入E装置被吸收.
解答 【实验探究一】①向盛有过碳酸钠固体的试管中加入适量水,目的是让过碳酸钠溶于水且能与水反应;
③根据题给条件可知,过碳酸钠溶于水时,反应生成碳酸钠和过氧化氢,向序号①的所得溶液中加入适量的二氧化锰粉末,产生了大量的气体,可使带火星的木条复燃,说明该气体是氧气,进一步说明了含有过氧化氢溶液;
④碳酸钠和氯化钙反应生成碳酸钙和氯化钠,方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl;
实验小结:由于过碳酸钠与水反应生成碳酸钠和过氧化氢,说明过碳酸钠中含氧量比碳酸钠高,并且过碳酸钠的相对分子质量为122;碳酸钠的相对分子质量为106,所以过碳酸钠应为Na2CO4;过碳酸钠与水反应的化学方程式为:Na2CO4+H2O=Na2CO3+H2O2;
【实验探究二】
(1)根据实验要求,组装好装置,检查气密性,装入药品,关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;称量装置E的质量,依次关闭活塞K1、K3、K4,打开活塞K2、K;关闭活塞K,打开活塞K1,通入氮气;再次称量装置E的质量.
(2)氢氧化钠可以与二氧化碳反应,除去空气中的二氧化碳,防止空气中的二氧化碳进入E装置;
(3)过碳酸钠溶于水时,反应生成碳酸钠和过氧化氢,过氧化氢在二氧化锰作用下生成水和氧气;碳酸钠与硫酸反应生成硫酸钠、水和二氧化碳;当气体通过浓硫酸时被干燥,通入E中装入碱石灰吸收其中的二氧化碳;实验完毕后通入氮气的目的是将装置中的气体排出,被E装置完全吸收;
(4)设该样品中过碳酸钠的质量为x,则碳酸钠的质量为:6.63g-x,
实验后E装置增重2.42g,说明反应生成了2.42g二氧化碳,
Na2CO4+H2O=Na2CO3+H2O2,Na2CO3+2HCl═2NaCl+H2O+CO2↑,
122 106 106 44
x $\frac{106x}{122}$ $\frac{106x}{122}+6.63g+x$ 2.42g
$\frac{106}{\frac{106x}{122}+6.63g+x}$=$\frac{44}{2.42g}$
x=6.1g,
该样品中过碳酸钠的含量为:$\frac{6.1g}{6.63g}$×100%=92%,
(5)F装入干燥的碱石灰,F装置可以防止空气中的二氧化碳和水蒸气进入E装置被吸收,这样E装置在测定前后的质量差值偏大,计算出了样品中碳酸钠的含量偏高,过碳酸钠的含量偏低.
故答案为:
| 序号 | 实验步骤 | 实验现象 | 实验分步结论(或解释) |
| ① | 向盛有过碳酸钠固体的试管中加入适量水 | 固体溶解 | 过碳酸钠易溶于水, 能与水发生反应. |
| ② | 向序号①的所得溶液中加入适量的二氧化锰粉末 | 有大量气泡 产生 | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ |
| ③ | 将带火星的木条置于试管口 | 木条复燃 | 序号②试管中产生的气体是 O2; 过碳酸钠溶于水能生成过氧化氢. |
| ④ | 取序号③试管中的上层清液加入氯化钙溶液 | 产生白色 沉淀 | 反应的化学方程式 Na2CO3+CaCl2═CaCO3↓+2NaCl. |
| 小结 | 过碳酸钠与水反应的化学方程式是 Na2CO4+H2O═Na2CO3+H2O2. | ||
点评 本题主要考查同学们的实验分析能力,难度较大,记住氧气的检验方法,掌握过氧化氢和碳酸钠的性质,能够根据物质的性质来选择合适的方法来对物质加以验证,其中检验碳酸盐常用的方法是用稀盐酸和氯化钙等.


科目:初中化学 来源: 题型:填空题
 物质的用途与其性质密切相关.
物质的用途与其性质密切相关.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
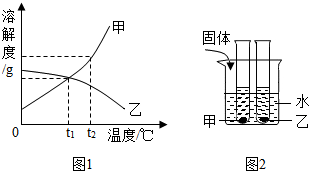 图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )
图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )| A. | t2℃时,甲、乙的饱和溶液中溶质的质量分数大小关系为甲>乙 | |
| B. | 甲、乙的饱和溶液分别从t2℃降至t1℃时,两溶液中溶质的质量分数大小关系为甲>乙 | |
| C. | 向烧杯的水中加NaOH固体后,乙溶液由饱和溶液变成不饱和溶液 | |
| D. | 向烧杯的水中加NH4NO3固体后,甲溶液溶质的质量分数减小 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
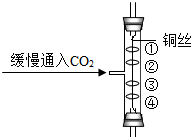
| A. | 只有①和② | B. | 都正确 | C. | 只有③和④正确 | D. | ②③④正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  | B. |  | ||
| C. |  | D. |  |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com