2.某化学兴趣小组在用高锰酸钾制取氧气的实验后,在清洗试管时发现试管内形成深绿色液体,同时试管内壁还有用水洗刷不掉的黑色固体.于是同学们对此展开探究.
问题一:黑色固体是什么?
【查阅资料】高锰酸钾能溶于水形成紫红色溶液.
【交流讨沦】同学们根据实验现象及对高锰酸钾受热分解产物的了解,推断该黑色固体可能是二氧化锰,其分子式为MnO
2.
【实验验证1】向未洗净的试管中加入某种液体,产生能使带火星的小木条复燃的气体,证明上述判断正确.加入的液体是双氧水.
问题二:用什么试剂洗掉MnO
2?
【交流讨论】MnO
2与CaCO
3、Mg(OH)
2、Fe
2O
3、P
2O
5、Cu中的某一种物质组成最相近,理由是二氧化锰和氧化铁都属于氧化物.
这种物质能与稀盐酸反应,观察到的现象应为固体逐渐溶解,溶液由无色变为黄色,由此推测MnO
2也能与稀盐酸反应.
【实验验证2】向未洗净的试管中加入稀盐酸,黑色固体没有变化.实验说明同一类物质的化学性质不一定相同.
【查阅资料】同学们查阅资料知道有两种除去二氧化锰的方法:
(1)用浓盐酸加热除去MnO
2,反应原理为:4HCl(浓)+MnO
2MnCl
2+Cl
2↑+2H
2O
(反应生成的氯气有毒).
(2)用硫酸酸化了的草酸(H
2C
2O
4)溶液,可快速溶解二氧化锰,且无明显现象.
【交流讨论】老师建议实验小组最好采用草酸溶液而不用浓盐酸进行实验,理由是浓盐酸与MnO
2在加热条件下反应不安全,且产生有毒气体氯气,对环境有污染.
【实验验证3】向未洗净的试管中加入硫酸酸化了的草酸溶液,黑色固体果然被除去,同时发现产生许多气泡.
【交流讨论】同学们讨论后认为产生的气体可能为CO
2、CO、H
2、O
2等.依据是化学反应前后元素的种类不发生变化.
【反思评价】经检验,产生的气体是CO
2.检验CO
2气体的实验操作和实验现象、结论是:
【拓展探究】甲、乙两位同学对草酸受热分解及其产物进行探究.
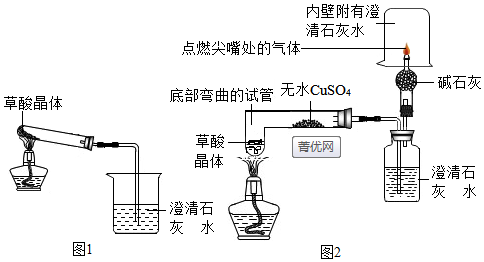
甲同学设计了如图1所示的装置,乙同学设计了如图2所示的装置(图中无水CuSO
4),是白色同体.遇水变蓝).乙同学认为甲同学设计的实验装置有缺陷:由于试管口向下倾斜.加之草酸晶体熔点较低.加热到182℃便开始熔化,因此实验中常会出现熔融的草酸流进导管而影响后续实验.甲同学认为乙同学的设计是科学合理的.请你谈谈图2装置优于图1装置之处:
①底部弯曲的试管避免了熔化的草酸流进导管;②乙同学设计的装置可同时证明二氧化碳、一氧化碳和水的存在;③乙同学的装置在验证了一氧化碳存在的同时又解决了一氧化碳的污染问题.
乙同学设计的图2装置也能证明产物中有无H
2,证明的方法是:在球形干燥管的尖嘴处点燃通过碱石灰干燥后的气体(或点燃尖嘴处的气体),并在火焰上方罩一冷而干燥的小烧杯,若烧杯内壁没有水雾出现,则没有氢气,反之,若烧杯内壁有水雾出现,则有氢气.

 名校课堂系列答案
名校课堂系列答案
