
分析 (1)根据物质结构决定物质的性质分析.金刚石的碳原子排列是空间网状结构,石墨的碳原子排列是层状结构;
(2)根据三种物质的组成、结构、性质分析;
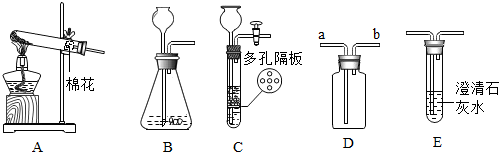
(3)①由于装置C可以通过固体和液体的分离与结合来控制反应的发生与停止,而B装置中药品加入后,不能分离,一旦发生就不能控制;
②二氧化碳与氢氧化钙反应生成碳酸钙和水,
③根据氢气的密度比空气小分析;
④如图所示实验装置属于固体加热型制取气体,且试管口有一团棉花,故是采用了加热高锰酸钾的方法制取氧气.
(4)碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,由参加反应的石灰石的质量、碳酸钙的质量分数,由反应的化学方程式列式计算出生成二氧化碳的质量
解答 解:(1)由于金刚石的碳原子排列是空间网状结构,石墨的碳原子排列是层状结构,金刚石、石墨的内部碳原子的排列方式不同,导致二种物质物理性质差异很大;
(2)①三种物质都含有碳元素,但是CO2不燃烧也不支持燃烧,故错误;
②CO、CO2都是没有颜色、没有气味的气体,故正确;
③CO2可用于光合作用,所以作为气体肥料,干冰可用于人工降雨,故错误;
④CO2能产生温室效应,CO易与血液中的血红蛋白结合引起中毒,故正确;
⑤CO2不燃烧也不支持燃烧,可用来灭火,CO具有可燃性,可用作燃料,故正确;
故选:C.
(3)①由于装置C可以通过固体和液体的分离与结合来控制反应的发生与停止,而B装置中药品加入后,不能分离,一旦发生就不能控制;故C装置的优点是:控制反应的发生与停止;
②二氧化碳与氢氧化钙发生反应生成碳酸钙沉淀和水,因此可观察到:澄清石灰水变浑浊.化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
③如用F装置收集H2,由于氢气的密度比空气小,则气体应从b端通入;
④高锰酸钾分解后生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(4)含碳酸钙80%的石灰石12.5g中含碳酸钙的质量为12.5g×80%=10g.
设生成二氧化碳的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
10g x
$\frac{100}{10g}=\frac{44}{x}$
x=4.4g.
答:生成二氧化碳的质量为4.4g
故答案为:(1)碳原子排列方式不同;(2)C;(3)①控制反应的发生与停止;②澄清石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O;③b;④2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;(4)4.4g.
点评 本题难度不大,掌握碳和碳的化合物的性质和气体的制备,利用化学方程式与溶质质量分数的综合计算即可正确解答本题,注意代入方程式计算的必须是纯物质的质量是正确解题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:选择题
| A. | 溶液具有均一性和稳定性,因为溶液中的各种粒子保持静止不动 | |
| B. | 饱和溶液是一定温度下不能再溶解该物质的溶液 | |
| C. | 不饱和溶液通过降低温度一定能变成饱和溶液 | |
| D. | 一种物质分散到另一种物质里一定能形成溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
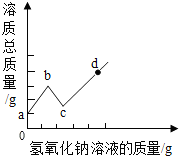 将某氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量:根据实验事实绘制如图所示曲线,请回答:
将某氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量:根据实验事实绘制如图所示曲线,请回答:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 已知A~F六种物质均为初中化学常见物质,其中B、E为氧化物,A、B、D、F为不同类别的化合物,A、B、D分别放入水中都能使酚酞溶液变红,如图是它们之间的关系(部分反应物和产物已省略;“→”表示转化,“-”表示相互反应).
已知A~F六种物质均为初中化学常见物质,其中B、E为氧化物,A、B、D、F为不同类别的化合物,A、B、D分别放入水中都能使酚酞溶液变红,如图是它们之间的关系(部分反应物和产物已省略;“→”表示转化,“-”表示相互反应).查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
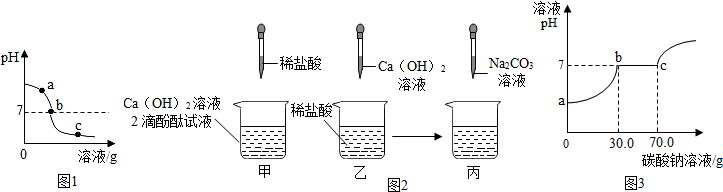
| 实验步骤 | 实验现象 | 实验结论 |
| 另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液. | ①只产生白色沉淀 | 该样品为b处溶液. |
| ②先产生气泡,后产生白色沉淀 | 该样品为c处溶液,并推知溶液中的阳离子有Ca2+、H+ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com