
【题目】下列关于金属的说法正确的是( )
A.人类使用金属铝的年代早于铜、铁
B.“真金不怕火炼”表明金(Au)在高温条件下也很难与氧气反应
C.通过高炉炼得的铁为纯铁
D.武德合金的熔点高,可用于制造保险丝
科目:初中化学 来源: 题型:
【题目】(10分)为探究气体X的组成,某兴趣小组进行图12所示实验(固定装置未画出)。
【资料在线】
(1)加热条件下,气体X能与氧化铜反应生成铜、水和氮气。
(2)碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应。
无水氯化钙可吸收气体X。
(3)本实验条件下,氮气密度为1.15g·L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计。
【实验步骤】
(1)连接仪器,并检查装置气密性。
(2)取一定量氧化铜,准确称得其质量为2.40g。
(3)按图12所示装入药品,测量并记录相关数据Ⅰ(见表1)。
(4)连接A、B、C装置, 将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热。当A装置中氧化铜反应完全,停止加热,继续通入气体 X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表1)。
【实验装置】
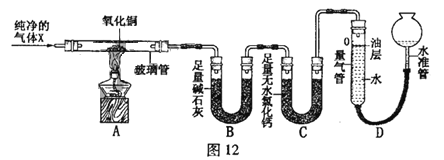
【相关数据】

【回答问题】
(1)B装置中氧化钙吸水的原理为 (用化学方程式表示)。
(2)实验过程中,当观察到 ,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是 。
(3)分析实验测量的数据,生成水的质量为 g,氧化铜中氧元素的质量为 g。
由此推知,气体X中一定 (填“有”或 “没有”)氧元素。
(4)通过计算推导出气体X的化学式。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组对实验室制取氢气的反应原理进行探究。
【知识回顾】能产生氢气的化学反应有: ①水电解 ②活泼金属与酸反应
【讨论交流】反应①的化学方程式 ;同学们讨论后认为该反应不适用于实验室制取氢气。
【实验探究】为了探究哪种物质更适合用于实验室制取氢气,大家设计了如下实验:
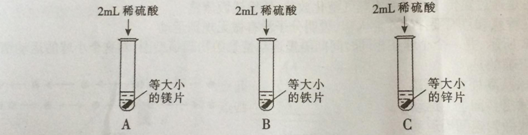
【分析与结论】填写实验报告。
实验 | 实验现象 | 实验结论 |
A | 剧烈反应,迅速产生大量气泡,试管外壁 | 反应速率过快,气体不便收集,不能用于实验室制取氢气 |
B | 缓慢产生少量气泡 | 反应速率过慢,不能用于实验室制取氢气 |
C | 较快产生大量气泡,试管外壁发热 |
通过实验得出,适合实验室制取氢气的化学反应方程式为 ;
【知识拓展】(1)确定实验室制取气体的反应原理时,要考虑诸多因素,如反应的快慢、收集的难易、 等。
(2)用稀盐酸制取氢气时,制得的气体中可能会增加的杂质为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(12分)二十一世纪是海洋开发与利用的世纪,我市实施黄蓝两大国家战略形成新的发展格局,海洋化学资源的综合利用将是重点发展领域之一。
(1)海水晒盐:将海水引入蒸发池,经日晒蒸发到一定程度时,导入结晶池,继续日晒,海水就会成为食盐的饱和溶液,再晒就会逐渐析出粗盐,剩余的液体称为母液(也称卤水)。
1L海水在逐渐浓缩过程中不断析出的盐的种类和质量(单位:g)关系如下表所示:
海水密度(g/mL) | CaSO4 | NaCl | MgCl2 | MgSO4 |
1.20 | 0.91 | |||
1.21 | 0.05 | 3.26 | 0.004 | 0.008 |
1.22 | 0.015 | 9.65 | 0.01 | 0.04 |
1.26 | 0.01 | 2.64 | 0.02 | 0.02 |
1.31 | 1.40 | 0.54 | 0.03 |
I、海水晒盐是 (选填“物理”或“化学”)变化,包含蒸发、 等过程。
II、若得到纯度较高的粗盐和含浓度较高的卤水,卤水的密度应控制在什么范围 ,原因是 。
(2)海水制镁:海水晒盐后,以其母液(卤水)和贝壳(主要成分是CaCO3)为原料制镁,其工艺流程如下图所示:
![]()
I、步骤①所加的碱应该是 (选填“氢氧化钠”或“石灰乳”),步骤②反应的化学方程式是 ;若要验证镁、铁、铜的活动性顺序,选择铁丝后,还要选择 、 两种溶液。
II、Mg(OH)2加热分解生成MgO和H2O,MgO是高熔点的化合物,某些阻燃剂(阻碍燃烧的物质)的有效成分是Mg(OH)2。你认为Mg(OH)2能够阻燃的原因可能是 (选填序号)
A.Mg(OH)2分解需要吸收大量的热,降低了可燃物的着火点
B.生成的氧化镁覆盖在可燃物表面,隔绝了空气
C.生成的水蒸气降低了可燃物周围氧气浓度
D.反应因吸热降低了环境温度,使可燃物不易达到着火点
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(10分)钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某补钙药剂说明书的部分信息如图所示。现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图像如下。请根据有关信息回答问题。

第1次 | 第3次 | 第4次 | |
加入盐酸的质量(g) | 20 | 20 | 20 |
剩余固体的质量(g) | 35 | a | 20 |
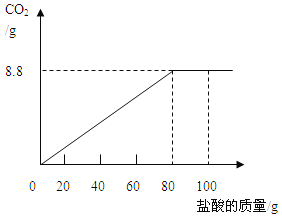
![]() (1)人体缺钙易出现的疾病是 ,这时除在医生指导下服用保健药剂外,日常生活中要多摄入 等食物。
(1)人体缺钙易出现的疾病是 ,这时除在医生指导下服用保健药剂外,日常生活中要多摄入 等食物。
(2)该品牌补钙药剂中CaCO3的质量分数是 ,a的数值为 。
(3)求该盐酸中溶质的质量分数为(写出计算过程,计算结果保留一位小数)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】右图为硝酸钾和氯化钠两种物质的饱和溶液的质量分数随温度变化的曲线,M、N分别是50℃时硝酸钾和氯化钠质量分数随温度变化曲线上的点。分析曲线得到的以下结论中,正确的是
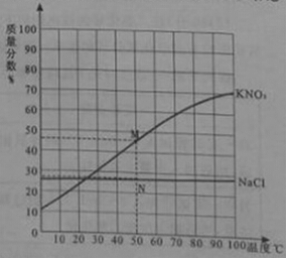
A.50℃时,M、N之间任一点表示的溶液一定是硝酸钾和氯化钠的饱和溶液
B.50℃时,其他条件不变,升温至60℃,M点向右平移,硝酸钾的溶解度增大
C.50℃时,其他条件不变,降温至40℃,N点向右平移,氯化钠的溶解度减小
D.50℃时,向两饱和溶液添加溶质,M点不动,硝酸钾和氯化钠的溶解度增大
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海洋是人类宝贵的自然资源,海水“制碱”体现了化学科学在改造物质中的智慧.
如图是某厂生产纯碱的工艺流程图:

请完成下列问题:
(1)流程Ⅰ中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是______________________(填字母序号);
A.加入三种溶液的顺序不能调整
B.加入三种溶液将粗盐水中的SO42﹣、Mg2+、Ca2+转化为沉淀
C.按流程Ⅰ所加溶液的顺序除杂,过滤后得到四种沉淀
(2)在流程Ⅰ中,加入BaCl2溶液时发生反应的化学方程式是______________________;
(3)在流程Ⅱ中,如果加入氨气不是为了生产氯化氨,氨气在制碱过程中的作用是__;
(4)写出流程Ⅲ中发生反应的化学方程式____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com