
| A. | 镍能与氯化铜溶液发生置换反应 | |
| B. | 反应③中X代表的物质是水 | |
| C. | 反应②和③都是复分解反应 | |
| D. | 反应中Ni①、③的化合价都发生了变化 |
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 胃液中少量的盐酸可以帮助消化 | |
| B. | 油脂使人肥胖,进食时要避免摄入脂肪 | |
| C. | 无机盐和水虽不能提供能量,却是人体必需的 | |
| D. | 香烟烟气中的CO会使血红蛋白携氧能力降低 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
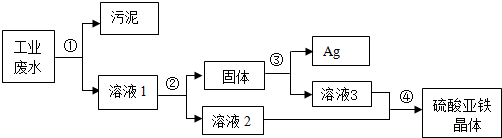
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
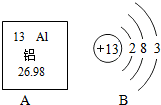 图A是铝元素在元素周期表中的部分信息,图B是铝原子的结构示意图,回答问题.
图A是铝元素在元素周期表中的部分信息,图B是铝原子的结构示意图,回答问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaC12溶液 |
| 实验操作 | 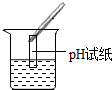 | 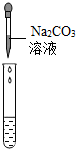 | 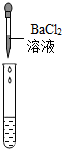 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 产生无色气泡 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com